هيكل أكسيد الكالسيوم (CaO) وخصائصه واستخداماته
ال أكسيد الكالسيوم (CaO) هو مركب غير عضوي يحتوي على الكالسيوم والأكسجين في أشكال أيونية (يجب عدم الخلط بينه وبين بيروكسيد الكالسيوم ، CaO2). ومن المعروف في جميع أنحاء العالم باسم الجير ، وهي الكلمة التي تحدد أي مركب غير عضوي يحتوي على الكربونات وأكاسيد الكالسيوم وهيدروكسيدات ، وكذلك المعادن الأخرى مثل السيليكون والألومنيوم والحديد..
يشار إلى هذا الأكسيد (أو الجير) أيضًا بالعامية باسم الجير المطفأ أو الجيري المائل ، اعتمادًا على ما إذا كان مرطبًا أم لا. الجير هو أكسيد الكالسيوم ، بينما الجير المكسور هو هيدروكسيده. بدوره ، الحجر الجيري (الحجر الجيري أو الجير المتصلب) هو في الواقع صخرة رسوبية تتكون أساسا من كربونات الكالسيوم (CaCO3).

إنه أحد أكبر مصادر الكالسيوم الطبيعية ويشكل المادة الخام لإنتاج أكسيد الكالسيوم. كيف يتم إنتاج هذا أكسيد؟ الكربونات عرضة للتحلل الحراري ؛ تسخين كربونات الكالسيوم في درجات حرارة أعلى من 825 درجة مئوية ، مما يؤدي إلى تكوين الجير وثاني أكسيد الكربون.
يمكن وصف البيان أعلاه على النحو التالي: CaCO3(s) → CaO (s) + CO2(G). لأن قشرة الأرض غنية بالحجر الجيري والكالسيت ، وفي المحيطات والشواطئ ، توجد قذائف بحرية وفيرة (المواد الخام لإنتاج أكسيد الكالسيوم) ، وأكسيد الكالسيوم كاشف رخيص نسبيا.
مؤشر
- 1 الصيغة
- 2 هيكل
- 3 خصائص
- 3.1 الذوبان
- 4 الاستخدامات
- 4.1 كقذيفة هاون
- 4.2 في إنتاج النظارات
- 4.3 في التعدين
- 4.4 كمزيل سيليكات
- 5 جسيمات نانوية من أكسيد الكالسيوم
- 6 المراجع
صيغة
الصيغة الكيميائية لأكسيد الكالسيوم هي CaO ، حيث يشبه الكالسيوم أيون الحمض (متقبل الإلكترون) Ca2+, والأكسجين كالأيون الأساسي (مانح الإلكترون) أو2--.
لماذا الكالسيوم لديه +2 تهمة؟ لأن الكالسيوم ينتمي إلى المجموعة 2 من الجدول الدوري (السيد Becambara) ، ويحتوي فقط اثنين من إلكترونات التكافؤ لتشكيل الروابط ، والتي تنتج إلى ذرة الأكسجين.
هيكل
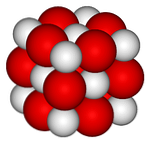
في الصورة العليا ، يتم تمثيل التركيب البلوري (نوع ملح الأحجار الكريمة) لأكسيد الكالسيوم. تتوافق المجالات الحمراء الضخمة مع أيونات الكالسيوم2+ والكرات البيضاء للأيونات O2-.
في هذا الترتيب البلوري المكعب كل Ca أيون2+ محاط بستة أيونات2-, تقع في الثقوب الثماني السطحية التي خلفتها أيونات كبيرة بينهما.
يعبر هذا الهيكل عن الحد الأقصى للشخصية الأيونية لهذا الأكسيد ، على الرغم من أن الاختلاف الملحوظ في نصف القطر (الكرة الحمراء أكبر من الكرة البيضاء) يمنح طاقة شبكية بلورية أضعف بالمقارنة مع MgO.
خصائص
جسديا ، إنها مادة صلبة بيضاء بلورية ، عديمة الرائحة ومع تفاعلات إلكتروستاتية قوية ، وهي المسؤولة عن نقاط الانصهار العالية (2572 درجة مئوية) والغليان (2850 درجة مئوية). بالإضافة إلى ذلك ، يبلغ وزنها الجزيئي 55،958 جم / مول وخاصية مثيرة للاهتمام لكونها مضيء حراريًا.
هذا يعني أن قطعة من أكسيد الكالسيوم المعرضة للهب يمكن أن تتألق بضوء أبيض كثيف ، المعروف باللغة الإنجليزية باسم الأضواء, أو باللغة الإسبانية ، ضوء الكالسيوم. أيونات الكالسيوم2+, في اتصال مع النار ، فإنها تسبب لهب محمر ، كما هو مبين في الصورة التالية.

الذوبانية
CaO هو أكسيد أساسي له صلة قوية بالماء ، لدرجة أنه يمتص الرطوبة (وهو عبارة عن مادة صلبة استرطابية) ، ويتفاعل فورًا لإنتاج الجير المقشور أو هيدروكسيد الكالسيوم:
CaO (s) + H2O (l) => Ca (OH)2(S)
هذا التفاعل طارد للحرارة (يطلق الحرارة) بسبب تكوين مادة صلبة ذات تفاعلات أقوى وشبكة بلورية أكثر استقرارًا. ومع ذلك ، يكون رد الفعل قابلاً للانعكاس إذا تم تسخين Ca (OH)2, تجفيفه وإضاءة الجير المائل ؛ ثم ، الجير "تولد من جديد".
المحلول الناتج أساسي للغاية ، وإذا كان مشبعًا بأكسيد الكالسيوم فإنه يصل إلى درجة حموضة قدرها 12.8.
وبالمثل ، فهو قابل للذوبان في الجلسرين وفي المحاليل الحمضية والسكرية. نظرًا لكونه أكسيدًا أساسيًا ، فإنه من الطبيعي أن يتفاعل بشكل فعال مع أكاسيد الحمض (SiO)2, ل2O3 والإيمان2O3, على سبيل المثال) أن تكون قابلة للذوبان في المراحل السائلة منه. من ناحية أخرى ، لا يذوب في الكحول والمذيبات العضوية.
تطبيقات
يحتوي CaO على عدد كبير من الاستخدامات الصناعية ، وكذلك في تخليق الأسيتيلين (CH≡CH) ، في استخراج الفوسفات من مياه الصرف الصحي وفي التفاعل مع ثاني أكسيد الكبريت من النفايات الغازية..
الاستخدامات الأخرى لأكسيد الكالسيوم موصوفة أدناه:
كهاون
إذا تم خلط أكسيد الكالسيوم بالرمل (SiO)2) والماء ، الكعك مع الرمل ويتفاعل ببطء مع الماء لتشكيل الجير المطحون. في المقابل ، فإن CO2 من الهواء يذوب في الماء ويتفاعل مع الملح قبالة لتشكيل كربونات الكالسيوم:
كاليفورنيا (أوهايو)2(ق) + CO2(g) => CaCO3(ق) + ح2يا (ل)
و CaCO3 وهو مركب أكثر صلابة وأكثر صلابة من CaO ، مما تسبب في هاون (الخليط السابق) لتصلب وإصلاح الطوب أو كتل أو السيراميك بينهما أو على السطح المطلوب.
في إنتاج النظارات
المواد الخام الأساسية لإنتاج النظارات هي أكاسيد السيليكون ، والتي يتم خلطها مع الجير ، كربونات الصوديوم (Na2CO3) وغيرها من المواد المضافة ، ثم تتعرض للتسخين ، مما يؤدي إلى مادة صلبة زجاجية. بعد ذلك يتم تسخين هذه المادة الصلبة وتفجيرها بأي شكل من الأشكال.
في التعدين
يحتل الجير المطفأ حجمًا أكبر من حجم الجير بسبب تفاعلات رابطة الهيدروجين (O-H-O). هذه الخاصية تستخدم لكسر الصخور من الداخل.
يتحقق ذلك عن طريق ملئها بمزيج مضغوط من الجير والماء ، وهو محكم الغلق لتركيز حرارته وقدرته الواسعة على الصخور..
كمزيل سيليكات
يتم تنصهر CaO مع السيليكات لتكوين سائل متماسك ، والذي يتم استخلاصه بعد ذلك من المادة الخام لمنتج معين.
على سبيل المثال ، خامات الحديد هي المادة الخام لإنتاج الحديد والصلب المعدني. تحتوي هذه المعادن على السيليكات ، وهي شوائب غير مرغوب فيها للعملية ويتم التخلص منها بالطريقة الموصوفة للتو.
الجسيمات النانوية من أكسيد الكالسيوم
يمكن تصنيع أكسيد الكالسيوم كجسيمات متناهية الصغر ، وتغيير تركيزات نترات الكالسيوم (Ca (NO3)2) وهيدروكسيد الصوديوم (هيدروكسيد الصوديوم) في محلول.
هذه الجسيمات كروية ، أساسية (وكذلك صلبة على نطاق واسع) ولها مساحة كبيرة من السطح. وبالتالي ، فإن هذه الخصائص تفيد العمليات الحفزية. ماذا؟ التحقيقات حاليا تجيب على هذا السؤال.
تم استخدام هذه الجسيمات النانوية لتوليف المركبات العضوية البديلة - المشتقة من البيريدين - في صياغة أدوية جديدة لتنفيذ التحولات الكيميائية مثل التمثيل الضوئي الاصطناعي ، لتنقية المياه من المعادن الثقيلة والضارة ، عوامل التحفيز الضوئي.
يمكن تصنيع الجسيمات النانوية على دعم بيولوجي ، مثل أوراق البابايا والشاي الأخضر ، لاستخدامها كعامل مضاد للجراثيم.
مراجع
- scifun.org. (2018). الجير: أكسيد الكالسيوم. تم الاسترجاع في 30 مارس 2018 من: scifun.org.
- ويكيبيديا. (2018). أكسيد الكالسيوم. تم الاسترجاع في 30 مارس 2018 من: en.wikipedia.org
- أشويني أنانثرامان وآخرون. (2016). التخليق الأخضر للجسيمات النانوية لأكسيد الكالسيوم وتطبيقاتها. المجلة الدولية للبحوث الهندسية والتطبيق. ISSN: 2248-9622 ، المجلد 6 ، العدد 10 ، (الجزء -1) ، الصفحات 27-31.
- J. Safaei-Ghomi et al. (2013). حفزت الجسيمات النانوية من أكسيد الكالسيوم تخليق مكون من خطوة واحدة لبيريدينات شديدة الاستبدال في وسط الإيثانول المائي Scientia Iranica، Transactions C: Chemistry and Chemical Engineering 20 549-554.
- بوب كيم. (2018). أكسيد الكالسيوم. تم الاسترجاع في 30 مارس 2018 من: pubchem.ncbi.nlm.nih.gov
- رعشة واتكينز. (2008). كيمياء غير عضوية في عناصر المجموعة 2. (الطبعة الرابعة ، صفحة 280). مولودية جراو هيل.


