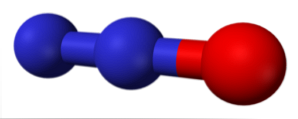
أكاسيد النيتروجين (NOx) تركيبات وصيغ مختلفة
ال أكاسيد النيتروجين هي عبارة عن مركبات غير عضوية غازية تحتوي على روابط بين ذرات النيتروجين والأكسجين. الصيغة الكيميائية لمجموعتها هي NOس, مما يشير إلى أن الأكاسيد لها نسب مختلفة من الأكسجين والنيتروجين.
يقود النيتروجين المجموعة 15 من الجدول الدوري ، في حين أن مجموعة الأكسجين 16 ؛ كلا العنصرين عضوان في الفترة 2. هذا التقارب هو السبب في أن روابط N-O تساهمية في الأكاسيد. بهذه الطريقة ، تكون الروابط في أكاسيد النيتروجين تساهمية.
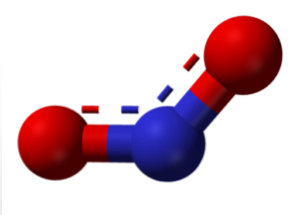
كل هذه الروابط يمكن تفسيرها باستخدام نظرية المدارية الجزيئية ، والتي تكشف عن المغنطيسية (إلكترون لم يسبق له مثيل في المدار الجزيئي الأخير) لبعض هذه المركبات. من هذه المركبات الأكثر شيوعًا هي أكسيد النيتريك وثاني أكسيد النيتروجين.
يتوافق الجزيء الموجود في الصورة العليا مع التركيب الزاوي في الطور الغازي لثاني أكسيد النيتروجين (NO2). في المقابل ، يحتوي أكسيد النيتريك (NO) على بنية خطية (مع مراعاة تهجين sp لكلتا الذرتين).
أكاسيد النيتروجين هي غازات تنتجها العديد من الأنشطة البشرية ، من قيادة السيارة أو تدخين السجائر إلى العمليات الصناعية كنفايات ملوثة. ومع ذلك ، يتم إنتاج NO بشكل طبيعي عن طريق التفاعلات الأنزيمية والبرق في العواصف الرعدية: N2(ز) + يا2(g) => 2NO (g)
درجات الحرارة العالية للأشعة تكسر حاجز الطاقة الذي يمنع حدوث هذا التفاعل في ظل الظروف العادية. ما حاجز الطاقة؟ التي تشكلت من الرابطة ثلاثية N≡N ، مما يجعل جزيء N2 غاز خامل من الجو.
مؤشر
- 1 أعداد الأكسدة للنيتروجين والأكسجين في أكاسيدهم
- 2 الصياغات المختلفة والتسميات
- 2.1 أكسيد النيتروز (N2O)
- 2.2 أكسيد النيتريك (NO)
- 2.3 ثالث أكسيد النيتروجين (N2O3)
- 2.4 ثاني أكسيد النيتروجين وثاني أكسيد النيتروجين (NO2، N2O4)
- 2.5 خامس أكسيد النيتروجين (N2O5)
- 3 المراجع
أعداد الأكسدة للنيتروجين والأكسجين في أكاسيدهم
التكوين الإلكتروني للأكسجين هو [He] 2s22P4, تحتاج فقط اثنين من الإلكترونات لاستكمال الثماني من قذيفة التكافؤ ؛ بمعنى أنه يمكن أن يكسب إلكترونين ويكون له رقم أكسدة يساوي -2.
من ناحية أخرى ، التكوين الإلكتروني للنيتروجين هو [He] 2s22P3, القدرة على الحصول على ما يصل إلى ثلاثة إلكترونات لملء الثماني التكافؤ ؛ على سبيل المثال ، في حالة الأمونيا (NH3) له رقم أكسدة يساوي -3. لكن الأكسجين أكثر إلكترونيا من الهيدروجين و "يجبر" النيتروجين على مشاركة إلكتروناته.
كم عدد الإلكترونات التي يمكن أن يشاركها النيتروجين مع الأكسجين؟ إذا قمت بمشاركة إلكترونات قذيفة التكافؤ الخاصة بك واحدة تلو الأخرى ، فستصل إلى الحد المسموح به وهو خمسة إلكترونات تقابل رقم الأكسدة +5.
وبالتالي ، بناءً على عدد الروابط التي يتكون منها الأكسجين ، تختلف أعداد أكسدة النيتروجين من +1 إلى +5.
تركيبات مختلفة و التسميات
أكاسيد النيتروجين ، بالترتيب المتزايد لأرقام أكسدة النيتروجين ، هي:
- N2أو أكسيد النيتروز (+1)
- لا ، أكسيد النيتريك (+2)
- N2O3, ثالث أكسيد النيتروجين (+3)
- NO2, ثاني أكسيد النيتروجين (+4)
- N2O5, خامس أكسيد النيتروجين (+5)
أكسيد النيتروز2O)
أكسيد النيتروز (أو المعروف باسم غاز الضحك) هو غاز عديم اللون ، مع رائحة حلوة طفيفة وردود الفعل قليلا. يمكن تصورها كجزيء ن2 (الكرات الزرقاء) التي أضافت ذرة الأكسجين في نهاية واحدة. يتم تحضيره بواسطة التحلل الحراري لأملاح النترات ويستخدم كمخدر ومسكن.
يحتوي النيتروجين على رقم أكسدة في +1 من هذا الأكسيد ، مما يعني أنه ليس مؤكسدًا للغاية وأن الطلب على الإلكترونات ليس مقنعًا ؛ ومع ذلك ، تحتاج فقط إلى كسب إلكترونين (واحد لكل نيتروجين) لتصبح نيتروجين جزيئي مستقر.
في المحاليل الأساسية والحمضية تكون التفاعلات:
N2يا (ز) + 2H+(ac) + 2e- => ن2(ز) + ح2يا (ل)
N2يا (ز) + ح2يا (ل) + 2e- => ن2(ز) + 2OH-(آق)
هذه التفاعلات ، على الرغم من أن الديناميكا الحرارية يفضلها تكوين جزيء مستقر N2, تحدث ببطء ويجب أن تكون الكواشف التي تتبرع بزوج الإلكترونات من عوامل الاختزال القوية للغاية.
أكسيد النيتريك (لا)
يتكون هذا أكسيد من غاز عديم اللون ، رد الفعل وشبه المغنطيسي. مثل أكسيد النيتروز ، له هيكل جزيئي خطي ، ولكن مع وجود فرق كبير أن الرابطة N = O لها أيضًا شخصية رابطة ثلاثية..
لا يتأكسد بسرعة في الهواء لإنتاج NO2, وبالتالي توليد المزيد من المدارات الجزيئية مستقرة مع ذرة النيتروجين أكثر أكسدة (+4).
2NO (g) + O2(ز) => 2NO2(G)
الدراسات الكيميائية والفيزيولوجية الحيوية وراء الدور الحميد لهذه الأكسيد في الكائنات الحية.
لا يمكن أن تشكل روابط N-N مع جزيء آخر من NO بسبب إلغاء تحديد موقع الإلكترون غير المزاوج في المدار الجزيئي ، والذي يتم توجيهه أكثر نحو ذرة الأكسجين (بسبب إرتفاع كهروته الإلكترونية). يحدث العكس مع NO2, يمكن أن تشكل الثغرات الغازية.
ثالث أكسيد النيتروجين (N2O3)
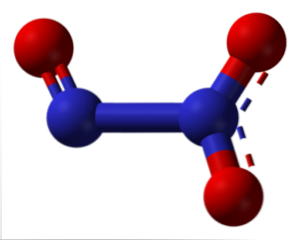
تشير الخطوط المنقطة للهيكل إلى رنين مزدوج للسندات. مثل كل الذرات ، لديهم تهجين س2, الجزيء مسطح والتفاعلات الجزيئية فعالة بما فيه الكفاية لثلاثي أكسيد النيتروجين في الوجود كمادة صلبة زرقاء تحت -101 درجة مئوية. في درجات الحرارة العالية يذوب وينفصل إلى NO و NO2.
لماذا هو فصل؟ نظرًا لأن أرقام الأكسدة +2 و +4 أكثر ثباتًا من +3 ، فإن الأخير موجود في أكسيد لكل من ذرات النيتروجين. هذا ، مرة أخرى ، يمكن تفسيره من خلال استقرار المدارات الجزيئية الناتجة عن عدم التناسب.
في الصورة ، الجانب الأيسر من N2O3 يتوافق مع NO ، في حين أن الجانب الأيمن من NO2. من الناحية المنطقية ، يتم إنتاجه عن طريق اندماج الأكاسيد السابقة في درجات حرارة شديدة البرودة (-20 درجة مئوية). ذا ن2O3 هو أنهيدريد حمض النيتروز (HNO2).
ثاني أكسيد النيتروجين وثاني أكسيد النيتروجين (NO2, N2O4)
NO2 إنه غاز بني أو بني ، تفاعلي وشبه مغناطيسي. نظرًا لأنه يحتوي على إلكترون غير متزاوج ، فإنه ينتقص (يربط) بجزيء غازي NO آخر2 لتشكيل رباعي أكسيد النيتروجين ، غاز عديم اللون ، مما يوازن بين النوعين الكيميائيين:
2NO2(G) <=> N2O4(G)
إنه عامل مؤكسد سام ومتعدد الاستخدامات ، قادر على عدم التناسب في تفاعلات الأكسدة والاختزال في الأيونات (الأكسان).2- و لا3- (توليد الأمطار الحمضية) ، أو في NO.
وبالمثل ، فإن NO2 يشارك في التفاعلات الجوية المعقدة التي تسبب اختلافات في تركيزات الأوزون (OR3) على المستويات الأرضية وفي الستراتوسفير.
خامس أكسيد النيتروجين (N2O5)
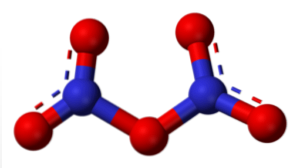
عندما رطب ، فإنه يولد HNO3, وعند تراكيز أعلى من الحمض ، يتأكس الأكسجين بشكل أساسي بشحنة موجبة جزئية- O+-H ، تسريع ردود الفعل الأكسدة
مراجع
- askIITians. ((2006-2018)). askIITians. تم الاسترجاع في 29 مارس 2018 ، من askIITians: askiitians.com
- موسوعة بريتانيكا ، شركة (2018). موسوعة بريتانيكا. تم الاسترجاع في 29 مارس 2018 من موسوعة بريتانيكا: britannica.com
- توكس تاون. (2017). توكس تاون. تم الاسترجاع في 29 مارس 2018 من مدينة توكس تاون: toxtown.nlm.nih.gov
- البروفيسور باتريشيا شبلي. (2010). أكاسيد النيتروجين في الجو. جامعة إلينوي. تم الاسترجاع في 29 مارس 2018 ، من: butane.chem.uiuc.edu
- رعشة واتكينز. (2008). كيمياء غير عضوية في عناصر المجموعة 15. (الطبعة الرابعة. ، ص. 361-366). مولودية جراو هيل