خصائص يودوات البوتاسيوم ، الهيكل ، الإستخدامات والمخاطر
ال يودات البوتاسيوم أو يودات البوتاسيوم هو مركب غير عضوي من اليود ، وعلى وجه التحديد ملح ، تركيبة كيميائية له هي KIO3. يحتوي اليود ، عنصر مجموعة الهالوجينات (F ، Cl ، Br ، I ، As) ، في هذا الملح على رقم أكسدة +5 ؛ بسبب هذا هو عامل مؤكسد قوي. و KIO3 ينفصل في وسط مائي لإنشاء أيونات K+ و IO3-.
يتم تصنيعه عن طريق تفاعل هيدروكسيد البوتاسيوم مع حمض اليودك: HIO3(aq) + KOH (s) => KIO3(أ ك) + ح2يا (ل) أيضا ، يمكن تصنيعه عن طريق تفاعل اليود الجزيئي مع هيدروكسيد البوتاسيوم: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2يا (ل).

مؤشر
- 1 الخصائص الفيزيائية والكيميائية
- 1.1 عامل مؤكسد
- 2 التركيب الكيميائي
- 3 استخدامات وتطبيقات يودات البوتاسيوم
- 3.1 الاستخدام العلاجي
- 3.2 استخدم في الصناعة
- 3.3 الاستخدام التحليلي
- 3.4 استخدم في تكنولوجيا الليزر
- 4 المخاطر الصحية من يودات البوتاسيوم
- 5 المراجع
الخصائص الفيزيائية والكيميائية
إنها مادة صلبة بيضاء عديمة الرائحة ، مع بلورات رفيعة وهيكل بلوري من النوع أحادي الميل. له كثافة 3.98 جم / مل ، وزن جزيئي قدره 214 جم / مول وله نطاقات امتصاص في طيف الأشعة تحت الحمراء (IR).
لديها نقطة انصهار: 833 ºK (560 ºC) ، بما يتوافق مع التفاعلات الأيونية القوية بين أيونات K+ و IO3-. في درجات الحرارة العالية ، فإنه يخضع لتفاعل التحلل الحراري ، والإفراج عن الأكسجين الجزيئي ويوديد البوتاسيوم:
2KIO3(s) => 2KI (s) + 3O2(G)
لها الذوبان في الماء تتراوح بين 4،74g / 100ML إلى 0 درجة مئوية، إلى 32.3 غرام / 100 مل إلى 100 ° C، وتوليد المحاليل المائية عديم اللون. وعلاوة على ذلك، فإنه غير قابل للذوبان في الكحول وحمض النيتريك، ولكن قابل للذوبان في حمض الكبريتيك المخفف.
إن تقاربها مع الماء ليس ملموسًا ، وهو ما يفسر سبب عدم رطوبة الجسم وعدم وجوده في شكل أملاح رطبة (KIO)3· ح2O).
عامل مؤكسد
يحتوي يودات البوتاسيوم ، كما هو مبين في صيغته الكيميائية ، على ثلاث ذرات أكسجين. هذا عنصر ذو قوة كهربية قوية ، وبسبب هذه الخاصية ، فإنه "يكتشف" نقصًا إلكترونيًا في السحابة المحيطة باليود.
ويمكن حساب هذا النقص، أو المدخلات، مثل الإفرادية حيث بلغ عدد أكسدة اليود (± 1، +2، +3، +5، +7)، ويجري +5 في حالة من هذا الملح.
ماذا يعني هذا؟ قبل أن يتمكن نوع قادر على إنتاج إلكتروناته ، يقبل اليود في شكله الأيوني (IO)3-) ليصبح اليود الجزيئي ويكون له رقم أكسدة يساوي 0.
بعد هذا التفسير ، يمكن تحديد أن يودات البوتاسيوم عبارة عن مركب مؤكسد يتفاعل بشدة مع عوامل الاختزال في العديد من تفاعلات الأكسدة والاختزال ؛ من بين كل هذه الأشياء ، يُعرف الشخص باسم ساعة اليود.
تتكون ساعة اليود من عملية الأكسدة والاختزال من الخطوات البطيئة والسريعة ، والتي تتميز فيها الخطوات السريعة بحل KIO3 في حامض الكبريتيك الذي يضاف النشا. بعد ذلك ، النشا - تم إنتاجه وترسيخه مرة واحدة بين نوع بنيته الأولى3-- سوف يتحول الحل من عديم اللون إلى الأزرق الداكن.
IO3- + 3 HSO3- → أنا- + 3 HSO4-
IO3- + 5 أنا- + 6 ساعات+ → 3 أنا2 + 3 ساعات2O
أنا2 + HSO3- + H2يا → 2 أنا- + HSO4- + 2 ساعة+ (الأزرق الداكن بسبب تأثير النشا)
التركيب الكيميائي
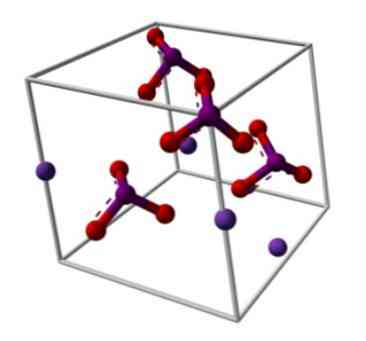
ويتضح الهيكل الكيميائي ليودات البوتاسيوم في الصورة العليا. أنيون IO3- ويمثلها "ترايبود" من المجالات الحمراء والارجوانية ، في حين أن الأيونات K+ ويمثلها المجالات الأرجواني.
ولكن ماذا تعني هذه حوامل؟ الأشكال الهندسية الصحيحة من هذه الشوارد هي في الواقع الأهرامات ثلاثي الزوايا، التي الأكسجين تشكل قاعدة مثلثة الشكل، والزوج غير مشترك من النقاط الإلكترونات اليود إلى أعلى، وتحتل مساحة وإجبار أضعاف أسفل الرابط IO واثنين الروابط I = O.
هذه الهندسة الجزيئية يتوافق مع تهجين sp3 من ذرة اليود المركزي ؛ ومع ذلك ، يشير منظور آخر إلى أن إحدى ذرات الأكسجين تشكل روابط مع المدارات "d" لليود ، في الواقع أنها تهجين sp3د2 (يمكن أن يشتمل اليود على مداراته "d" لتوسيع قشرة التكافؤ).
يمكن أن تمر بلورات هذا الملح بتحولات في المرحلة الهيكلية (ترتيبات أخرى غير أحادية السطح) كنتيجة لمختلف الظروف المادية التي تعرضها.
استخدامات وتطبيقات يودات البوتاسيوم
الاستخدام العلاجي
يودات البوتاسيوم عادة ما تستخدم لمنع تراكم النشاط الإشعاعي في الغدة الدرقية في شكل 131أنا ، عندما يتم استخدام هذا النظير في تحديد امتصاص الغدة الدرقية من قبل الغدة الدرقية كعنصر من عناصر أداء الغدة الدرقية.
وبالمثل ، يستخدم يودات البوتاسيوم كمطهر موضعي (0.5 ٪) في الالتهابات المخاطية.
استخدام في هذه الصناعة
يضاف إلى علف حيوانات المزرعة كمكمل لليود. لذلك ، في صناعة يودات البوتاسيوم يستخدم لتحسين نوعية الدقيق.
الاستخدام التحليلي
في الكيمياء التحليلية ، بفضل ثباتها ، يتم استخدامها كمعيار أساسي في توحيد المحاليل القياسية ثيوكبريتات الصوديوم (Na2S2O3) ، من أجل تحديد تركيزات اليود في العينات.
هذا يعني أنه يمكن معرفة كميات اليود من خلال التقنيات الحجمي (المعايرة). في هذا التفاعل ، أكسدة البوتاسيوم تتأكسد بسرعة أيونات iodide I-, بالمعادلة الكيميائية التالية:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
اليود ، أنا2, بعنوان حل Na2S2O3 لتوحيدها.
استخدامها في تكنولوجيا الليزر
وقد أظهرت الدراسات وأكدت اهتمام خصائص كهرضغطية، كهربي حراري، electrooptical، بلورات متعلق بالعازل الكهربائي الشفاف وغير الخطية البصريات مكتب الاستثمار الكويتي3. ينتج عن هذا إمكانات كبيرة في المجال الإلكتروني وفي تقنية الليزر للمواد المصنوعة من هذا المركب.
المخاطر الصحية لليودات البوتاسيوم
في الجرعات العالية يمكن أن يسبب تهيج في الغشاء المخاطي للفم والجلد والعينين والجهاز التنفسي.
وقد سمحت تجارب سمية يود البوتاسيوم في الحيوانات أن نلاحظ أن في الصيام الكلاب عند تناول جرعات من 0،2 حتي 0،25 جم / كجم من وزن الجسم، وتسليمها عن طريق الفم، فإنه يسبب القيء مجمع.
إذا تم تجنب هذه القيء ، فإنه يؤدي إلى تفاقم الوضع في الحيوانات ، لأنه يسبب فقدان الشهية والسجود قبل الموت. سمح تشريح جثته بمراقبة الآفات الميتة في الكبد والكلى والغشاء المخاطي في الأمعاء.
نظرًا لقوتها المؤكسدة ، فإنها تمثل خطر نشوب حريق عند ملامسة المواد القابلة للاشتعال.
مراجع
- اليوم ، R. ، و Underwood ، A. كيمياء تحليلية كمية (الطبعة الخامسة). بيرسون برنتيس هول ، ص -364.
- Muth، D. (2008). الليزر. تم الاسترجاع من: flickr.com
- ChemicalBook. (2017). يودات البوتاسيوم. تم الاسترجاع في 25 مارس 2018 ، من ChemicalBook: chemicalbook.com
- بوب كيم. (2018). يودات البوتاسيوم. تم الاسترجاع في 25 مارس 2018 ، من PubChem: pubchem.ncbi.nlm.nih.gov
- ميرك. (2018). يودات البوتاسيوم. تم الاسترجاع في 25 مارس 2018 من Merck:
- merckmillipore.com
- ويكيبيديا. (2017). يودات البوتاسيوم. تم الاسترجاع في 25 مارس 2018 ، من ويكيبيديا: en.wikipedia.org
- م محمد عبد القادر وآخرون. (2013). آلية نقل الشحن والتحولات في طور درجات الحرارة المنخفضة في KIO3. J. Phys.: Conf. Ser. 423 012036


