حمض الهيدروبروميك (HBr) هيكل ، والخصائص ، وتشكيل ، والاستخدامات
ال حمض الهيدروبروميك هو مركب غير عضوي ينتج عن المحلول المائي لغاز يسمى بروميد الهيدروجين. تركيبة كيميائية لها هي HBr ، ويمكن اعتبارها بطرق مختلفة مكافئة: مثل هيدريد جزيئي ، أو هاليد هيدروجين في الماء ؛ وهذا هو ، هيدرازيد.
في المعادلات الكيميائية ، يجب كتابتها كـ HBr (ac) ، للإشارة إلى أنه حمض هيدروبروميك وليس غازًا. هذا الحمض هو واحد من أقوى حمض الهيدروكلوريك ، حتى حمض الهيدروكلوريك. يكمن تفسير هذا في طبيعة الرابطة التساهمية.
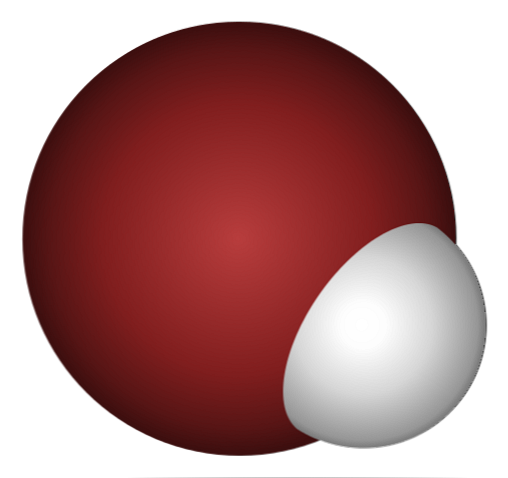
لماذا HBr مثل هذا الحمض ، وحتى أكثر يذوب في الماء؟ لأن الرابطة التساهمية H-Br ضعيفة للغاية ، بسبب التداخل الضعيف للمدارات 1 لـ H و 4 p لل Br.
هذا ليس مفاجئًا إذا نظرت عن كثب إلى الصورة أعلاه ، حيث من الواضح أن ذرة البروم (البني) أكبر بكثير من ذرة الهيدروجين (أبيض).
وبالتالي ، فإن أي اضطراب يتسبب في انهيار رابطة H-Br ، مما يؤدي إلى إطلاق H+. بعد ذلك ، فإن حمض الهيدروبروميك هو حمض برونستيد ، لأنه ينقل البروتونات أو أيونات الهيدروجين. قوتها بحيث يتم استخدامها في تخليق العديد من المركبات البروم العضوية (مثل 1-برومو الإيثان ، CH3CH2ر).
يعد حمض الهيدروبروميك ، بعد الهيدروكربون ، HI ، أحد أقوى الهيدروكربونات وأكثرها فائدة لهضم عينات صلبة معينة.
مؤشر
- 1 هيكل حمض الهيدروبروميك
- 1.1 الحموضة
- 2 الخصائص الفيزيائية والكيميائية
- 2.1 الصيغة الجزيئية
- 2.2 الوزن الجزيئي
- 2.3 المظهر الجسدي
- 2.4 الرائحة
- 2.5 عتبة الرائحة
- 2.6 الكثافة
- 2.7 نقطة انصهار
- 2.8 نقطة الغليان
- 2.9 الذوبان في الماء
- 2.10 كثافة البخار
- 2.11 pKa الحموضة
- 2.12 قدرة السعرات الحرارية
- 2.13 enthalpy المولي القياسية
- 2.14 الانتروبيا المولية
- 2.15 نقطة فلاش
- 3 تسميات
- 4 كيف يتم تشكيلها?
- 4.1 مزيج من الهيدروجين والبروم في الماء
- 4.2 الفوسفور ثلاثي البروميد
- 4.3 ثاني أكسيد الكبريت والبروم
- 5 الاستخدامات
- 5.1 تحضير البروميد
- 5.2 توليف هاليدات الألكيل
- 5.3 محفز
- 6 المراجع
هيكل حمض الهيدروبروميك
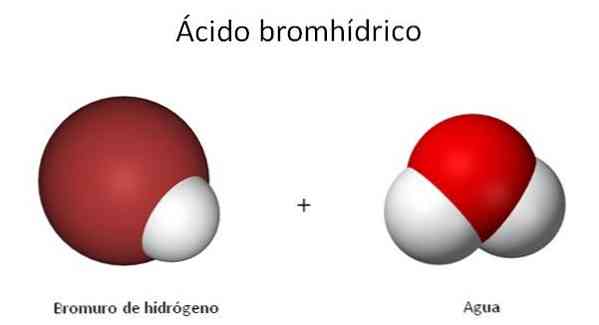
يظهر هيكل H-Br في الصورة ، حيث ترتبط خواصها وخصائصها ، حتى خصائص الغاز ، ارتباطًا وثيقًا بمحلولها المائي. هذا هو السبب في أن هناك نقطة حيث تحصل في حيرة حول أي من المركبين يتم الإشارة إليهما: HBr أو HBr (ac).
يختلف هيكل HBr (ac) عن هيكل HBr ، لأن جزيئات الماء تعمل الآن على إذابة هذا الجزيء ثنائي الذرة. عندما تكون قريبة بما فيه الكفاية ، يتم نقل H+ إلى جزيء H2أو كما هو مبين في المعادلة الكيميائية التالية:
HBr + H2يا => برا-- + H3O+
وبالتالي ، فإن هيكل حمض الهيدروبروميك يتكون من أيونات Br-- و ح3O+ التفاعل الكهربائي الآن ، يختلف الأمر قليلاً عن الرابطة التساهمية لـ H-Br.
حموضة كبيرة ويرجع ذلك إلى أنيون ضخمة- يمكن بالكاد التفاعل مع H3O+, غير قادر على منعه من نقل H+ إلى الأنواع الكيميائية المحيطة الأخرى.
خميرة
على سبيل المثال ، Cl- و F- على الرغم من أنها لا تشكل روابط تساهمية مع H3O+, يمكن أن تتفاعل من خلال قوى الجزيئات الأخرى ، مثل جسور الهيدروجين (والتي فقط F- قادر على قبولهم). جسور الهيدروجين F--H-OH2+ "تعيق" تبرع H+.
ولهذا السبب فإن حمض الهيدروفلوريك ، HF ، هو حمض أضعف في الماء من حمض الهيدروبروميك. منذ ذلك الحين ، التفاعلات الأيونية Br- H3O+ لا تهتم نقل H+.
ومع ذلك ، على الرغم من وجود الماء في HBr (ac) ، فإن سلوكه في نهاية الحساب يشبه سلوك جزيء H-Br ؛ وهذا هو ، ح+ يتم نقله من HBr أو Br-H3O+.
الخصائص الفيزيائية والكيميائية
الصيغة الجزيئية
دورية هارفارد.
الوزن الجزيئي
80972 جم / مول. لاحظ أنه ، كما ذكر في القسم السابق ، يعتبر HBr فقط وليس جزيء الماء. إذا تم أخذ الوزن الجزيئي من الصيغة Br-H3O+ سيكون لها قيمة 99 جم / مول تقريبًا.
المظهر الجسدي
سائل أصفر عديم اللون أو شاحب ، والذي سيعتمد على تركيز HBr المذاب. كلما كان لونها أصفر ، كلما كانت أكثر تركيزًا وخطورة.
رائحة
Acrid ، غضب.
رائحة العتبة
6.67 ملغ / م3.
كثافة
1.49 جم / سم3 (محلول مائي بنسبة 48 ٪ ث / ث). هذه القيمة ، مثل تلك المقابلة لنقاط الانصهار والغليان ، تعتمد على مقدار HBr المذاب في الماء.
نقطة انصهار
-11ºC (12ºF ، 393ºK) (محلول مائي عند 49 ٪ وزن / وزن).
نقطة الغليان
122 درجة مئوية (252 درجة فهرنهايت 393 درجة مئوية) عند 700 مم زئبق (محلول مائي 47-49٪ وزن / وزن).
الذوبان في الماء
-221 جم / 100 مل (عند 0 درجة مئوية).
-204 جم / 100 مل (15 درجة مئوية).
-130 جم / 100 مل (100 درجة مئوية).
تشير هذه القيم إلى HBr الغازي ، وليس إلى حمض الهيدروبروميك. كما يمكن أن يرى ، فإن زيادة درجة الحرارة تقلل من قابلية ذوبان HBr ؛ السلوك الطبيعي في الغازات. وبالتالي ، إذا كانت حلول HBr (ac) المركزة مطلوبة ، فمن الأفضل العمل معها في درجات حرارة منخفضة.
إذا كان يعمل في درجات حرارة عالية ، فسوف يهرب HBr في شكل جزيئات ثنائية الذرة الغازية ، لذلك يجب إغلاق المفاعل لمنع التسرب.
كثافة البخار
2.71 (فيما يتعلق بالهواء = 1).
الحموضة pKa
-9.0. هذا الثابت السلبي للغاية يدل على قوة حموضة كبيرة.
قدرة السعرات الحرارية
29.1 كيلو جول / مول.
مولان القياسية
198.7 كيلو جول / مول (298 كرونة).
الكون المولي القياسي
-36.3 كيلو جول / مول.
نقطة الاشتعال
غير قابلة للاشتعال.
تسمية
يجمع اسم "حمض الهيدروبروميك" بين حقيقتين: وجود الماء ، وهذا البروم يحتوي على تكافؤ -1 في المركب. في اللغة الإنجليزية ، يكون الأمر أكثر وضوحًا: حمض الهيدروبروميك ، حيث تشير البادئة "هيدرو" (أو هيدرو) إلى الماء ؛ على الرغم من أنه يمكن أن يشير أيضًا إلى الهيدروجين.
يحتوي البروم على تكافؤ -1 لأنه مرتبط بذرة الهيدروجين أقل كهربيًا منه ؛ ولكن إذا كانت مرتبطة أو تتفاعل مع ذرات الأكسجين ، فيمكن أن تحتوي على العديد من التكافؤ ، مثل: +2 ، +3 ، +5 و +7. مع H يمكن فقط اعتماد التكافؤ واحد ، وهذا هو السبب يضاف لاحقة -ico لاسمها.
في حين أن HBr (g) ، بروميد الهيدروجين ، لا مائي ؛ وهذا هو ، ليس لديها ماء. لذلك ، تم تسميته وفقًا لمعايير التسمية الأخرى ، المقابلة لتلك الخاصة بهاليدات الهيدروجين.
كيف يتم تشكيلها?
هناك عدة طرق اصطناعية لتحضير حمض الهيدروبروميك. البعض منهم:
مزيج من الهيدروجين والبروم في الماء
بدون وصف التفاصيل الفنية ، يمكن الحصول على هذا الحمض من المزيج المباشر من الهيدروجين والبروم في مفاعل مملوء بالماء.
H2 + ر2 => HBr
بهذه الطريقة ، عندما يتشكل HBr ، يذوب في الماء ؛ يمكن أن يسحبه في التقطير ، لذلك يمكن استخراج المحاليل بتركيزات مختلفة. الهيدروجين غاز ، والبروم سائل محمر داكن.
الفوسفور تريبروميد
في عملية أكثر تفصيلا ، يتم خلط الرمل والفوسفور الأحمر المائي والبروم. يتم وضع مصائد المياه في حمامات الجليد لمنع HBr من الهروب وتشكيل ، بدلا من ذلك ، حمض الهيدروبروميك. ردود الفعل هي:
2P + 3Br2 => 2PBr3
PBR3 + 3H2O => 3HBr + H3PO3
ثاني أكسيد الكبريت والبروم
هناك طريقة أخرى لإعداده وهي تفاعل البروم مع ثاني أكسيد الكبريت في الماء:
ر2 + SW2 + 2H2O => 2HBr + H2SW4
هذا هو رد فعل الأكسدة والاختزال. ذا برا2 أنه يقلل ، ويكسب الإلكترونات ، من خلال الربط مع الهيدروجين. بينما SO2 يتأكسد ، ويفقد الإلكترونات ، عندما يشكل روابط تساهمية أكثر مع أكسجين آخر ، كما هو الحال في حمض الكبريتيك.
تطبيقات
تحضير البروميد
يمكن تحضير أملاح البروميد إذا تفاعل HBr (ac) مع هيدروكسيد فلز. على سبيل المثال ، يعتبر إنتاج بروميد الكالسيوم:
كاليفورنيا (أوهايو)2 + 2HBr => CaBr2 + H2O
مثال آخر على بروميد الصوديوم:
NaOH + HBr => NaBr + H2O
وبالتالي ، يمكن تحضير العديد من البروميدات غير العضوية.
توليف هاليدات الألكيل
وماذا عن البروميدات العضوية؟ هذه مركبات برومينية: RBr أو ArBr.
الجفاف من الكحول
المواد الخام للحصول عليها يمكن أن تكون الكحول. عندما يتم البروتون بواسطة حموضة HBr ، فإنها تشكل ماء ، وهي مجموعة صادرة جيدة ، وبدلاً من ذلك يتم دمج الذرة الضخمة لـ Br ، والتي ستصبح مرتبطة بالتساهمي بالكربون:
ROH + HBr => RBr + H2O
يتم إجراء هذا الجفاف عند درجات حرارة أعلى من 100 درجة مئوية ، من أجل تسهيل تمزق رابطة R-OH2+.
بالإضافة إلى الألكينات والألكينات
يمكن إضافة جزيء HBr من محلوله المائي إلى رابطة مزدوجة أو ثلاثية من ألكين أو ألكين:
R2C = CR2 + HBr => RHC-CRBr
RC≡CR + HBr => RHC = CRBr
يمكن الحصول على العديد من المنتجات ، ولكن في ظل ظروف بسيطة ، يتم تكوين المنتج أولاً حيث يرتبط البروم بكربون ثانوي أو ثلاثي أو رباعي (قاعدة ماركوفنيكوف).
تتداخل هذه الهاليدات في تخليق المركبات العضوية الأخرى ، ومدى استخدامها واسع للغاية. أيضًا ، يمكن استخدام بعضها في تصنيع أو تصميم أدوية جديدة.
شق أثيري
من الإيثرات ، يمكن الحصول على هاليدات ألكيل في وقت واحد ، يحمل كل منهما أحد السلاسل الجانبية R أو R 'للأثير الأولي R-O-R'. يحدث شيء مشابه لجفاف الكحول ، لكن آلية تفاعله مختلفة.
يمكن تخطيط التفاعل باستخدام المعادلة الكيميائية التالية:
ROR '+ 2HBr => RBr + R'Br
ويصدر الماء أيضا.
الحفاز
الحموضة الخاصة به هي بحيث يمكن استخدامه كعامل مساعد فعال للحمض. بدلا من إضافة Br أنيون- إلى التركيب الجزيئي ، يفتح الطريق أمام جزيء آخر للقيام بذلك.
مراجع
- غراهام سولومونز تي. دبليو ، كريج بي فرايل. (2011). الكيمياء العضوية. الأمينات. (10عشر طبعة). وايلي بلس.
- كاري ف. (2008). الكيمياء العضوية (الطبعة السادسة). مولودية جراو هيل.
- ستيفن هاردينجر. (2017). مسرد مصور للكيمياء العضوية: حمض الهيدروبروميك. تم الاسترجاع من: chem.ucla.edu
- ويكيبيديا. (2018). حمض الهيدروبروميك. تم الاسترجاع من: en.wikipedia.org
- بوب كيم. (2018). حمض الهيدروبروميك. تم الاسترجاع من: pubchem.ncbi.nlm.nih.gov
- المعهد الوطني للسلامة والنظافة في العمل. (2011). بروميد الهيدروجين [PDF]. تم الاسترجاع من: insht.es
- PrepChem. (2016). إعداد حمض الهيدروبروميك. تم الاسترجاع من: prepchem.com


