السترونتيوم هيدروكسيد (Sr (OH) structure) التركيب الكيميائي وخصائصه واستخداماته
ال هيدروكسيد السترونتيوم (Sr (OH) ₂) هو مركب كيميائي غير عضوي يتكون من أيون السترونتيوم (Sr) واثنين من أيونات الهيدروكسيد (OH). يتم الحصول على هذا المركب من خلال الجمع بين ملح السترونتيوم مع قاعدة قوية ، مما يؤدي إلى مركب ذو طبيعة قلوية يكون تركيبته الكيميائية هي Sr (OH)2.
بشكل عام ، يتم استخدام هيدروكسيد الصوديوم (هيدروكسيد الصوديوم) أو هيدروكسيد البوتاسيوم (KOH) كقاعدة قوية لإعداد هيدروكسيد السترونتيوم. من ناحية أخرى ، فإن ملح السترونتيوم (أو أيون السترونتيوم) الذي يتفاعل مع القاعدة القوية هو نترات السترونتيوم Sr (NO3)2 وتوصف العملية بالتفاعل الكيميائي التالي:
2KOH + Sr (NO3)2 → 2KNO3 + Sr (OH)2
في حل الكاتيون السترونتيوم (الأب+) على اتصال مع أنيون هيدروكسيد (OH-) تشكيل ملح أيوني أساسي من السترونتيوم. نظرًا لأن السترونتيوم عبارة عن فلز قلوي ، فإن هيدروكسيد السترونتيوم يعتبر مركبًا قلويًا كاويًا.
مؤشر
- 1 الحصول عليها
- 2 التركيب الكيميائي والخصائص الفيزيائية والكيميائية
- 2.1 السترونتيوم هيدروكسيد Octahydrate
- 2.2 سترويدوم هيدروكسيد مونوهيدرات
- 2.3 هيدروكسيد السترونتيوم اللامائي
- 2.4 الذوبان
- 2.5 التفاعل الكيميائي
- 3 الاستخدامات
- 3.1 استخراج دبس السكر وتكرير بنجر السكر
- 3.2 دهون السترونتيوم
- 3.3 استقرار البلاستيك
- 3.4 تطبيقات أخرى
- 4 المراجع
الحصول على
بالإضافة إلى العملية الموضحة سابقًا ، يمكن القول أنه بمجرد تنفيذ التفاعل ، Sr (OH)2 يترسب في الحل. ثم تخضع لعملية الغسيل والتجفيف ، وأخيراً تحصل على مسحوق أبيض ناعم جدًا.
طريقة بديلة للحصول على هيدروكسيد السترونتيوم هي من تسخين كربونات السترونتيوم (SrCO)3) أو كبريتات السترونتيوم (SrSO)4) مع البخار عند درجة حرارة تتراوح بين 500 درجة مئوية و 600 درجة مئوية. يحدث التفاعل الكيميائي كما هو موضح أدناه:
SrCO3 + H2يا → Sr (OH)2 + CO2
SRS + 2H2يا → Sr (OH)2 + H2S
التركيب الكيميائي و الخواص الفيزيائية الكيميائية
في الوقت الحاضر ، هناك 3 أشكال من هيدروكسيد السترونتيوم معروفة: الأوكتاهيدرات ، مونوهيدرات واللامائي.
السترونتيوم هيدروكسيد Octahydrate
من المحاليل تحت الظروف العادية لدرجات الحرارة والضغط (25 درجة مئوية و 1 ذرة) ، يترسب هيدروكسيد السترونتيوم في شكل ثماني الشكل ، صيغته الكيميائية هي Sr (OH)2∙ 8H2O.
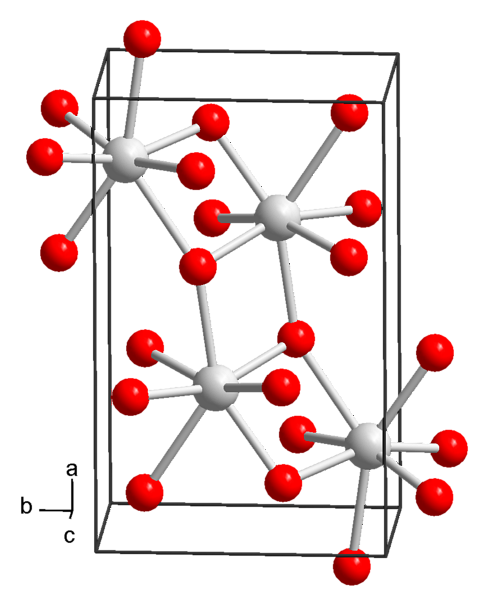
يحتوي هذا المركب على كتلة مولارية تبلغ 265.76 جم / مول ، وكثافة 1.90 جم / سم ويرسب كبلورات رباعي الزوايا (مع مجموعة فضاء P4 / ncc) ذات مظهر موشوري رباعي الزوايا وعديم اللون.
أيضا ، فإن هيدروكسيد سترونتيوم الأوكتاهيدرات لديه القدرة على امتصاص الرطوبة في الغلاف الجوي ، لأنه مركب سهل الذوبان.
السترونتيوم هيدروكسيد مونوهيدرات
وفقًا لدراسات الفحص المجهري البصري (التي أجريت باستخدام تقنية حيود الأشعة السينية) ، عن طريق رفع درجة الحرارة إلى حوالي 210 درجة مئوية - عند ضغط جوي ثابت - Sr (OH)2∙ 8H2أو يتم تجفيفه وتحويله إلى مونوهيدرات سترونتيوم هيدروكسيد (Sr (OH)2∙ ح2O).
هذا النوع من المركب له كتلة مولية قدرها 139.65 جم / مول ودرجة حرارة الانصهار هي -73.15 درجة مئوية (375K). نظرًا لتكوينها الذري ، فإنها تقدم ذوبانًا أقل في الماء عن تلك الموصوفة في شكلها الثماني.
هيدروكسيد السترونتيوم اللامائي
من خلال الاستمرار في زيادة درجة حرارة النظام إلى حوالي 480 درجة مئوية ، يستمر الجفاف حتى يتم الحصول على هيدروكسيد السترونتيوم اللامائي.
على عكس أشكاله الرطبة ، فإن الكتلة المولية لها 121.63 جم / مول وكثافة 3.625 جم / سم3. يتم الوصول إلى نقطة الغليان عند 710 درجة مئوية (1،310 درجة فهرنهايت أو 983 كلفن) بينما نقطة الانصهار هي عند 535 درجة مئوية (995 درجة فهرنهايت أو 808 درجة مئوية).
الذوبانية
يحتوي هيدروكسيد ثماني الهيدرات من السترونتيوم على ذوبان في الماء يبلغ 0.91 جرام لكل 100 مليلتر (يقاس عند 0 درجة مئوية) ، في حين أن شكله اللامائي في ظروف درجة حرارة مماثلة لديه قابلية ذوبان 0.41 جرام لكل 100 مل.
بنفس الطريقة ، تعتبر هذه المادة غير قابلة للذوبان في الأسيتون وقابلة للذوبان تمامًا في الأحماض وكلوريد الأمونيوم.
التفاعل الكيميائي
هيدروكسيد السترونتيوم غير قابل للاشتعال ، ويظل تفاعله الكيميائي مستقراً في درجات الحرارة والضغط المعتدلين ، وهو قادر على امتصاص ثاني أكسيد الكربون من الهواء الجوي ، وتحويله إلى كربونات السترونتيوم.
بالإضافة إلى ذلك ، فهو مركب مزعج للغاية إذا كان في اتصال مع الجلد أو الجهاز التنفسي أو غيرها من المناطق المخاطية في الجسم.
تطبيقات
بسبب خصائصه الرطبة وخصائصه الأساسية ، يستخدم هيدروكسيد السترونتيوم في تطبيقات مختلفة في الصناعة:
- استخراج دبس السكر وتكرير السكر من البنجر.
- استقرار البلاستيك.
- الشحوم وزيوت التشحيم.
استخراج دبس السكر وتكرير بنجر السكر
في بداية القرن الحادي والعشرين ، استخدم هيدروكسيد السترونتيوم في ألمانيا لتكرير السكر من البنجر من خلال العملية التي حصل عليها كارل شيبلر في عام 1882..
تتكون هذه العملية من خلط هيدروكسيد السترونتيوم ولب السكر في البنجر ، مما ينتج عنه ثنائي السكاريد غير القابل للذوبان. يتم فصل هذا المحلول عن طريق الصب ، وبمجرد إجراء عملية التكرير ، يتم الحصول على السكر كمنتج نهائي.
على الرغم من أن هذا الإجراء لا يزال يستخدم حتى اليوم ، إلا أن هناك طرقًا أخرى ذات طلب أكبر بكثير ، لأنها أرخص ، وتستخدم في الغالبية العظمى من مصافي السكر في العالم. على سبيل المثال ، طريقة Barsil ، التي تستخدم سيليكات الباريوم أو طريقة ستيفن باستخدام كال كعامل مستخرج.
شحوم السترونتيوم
إنها شحوم تشحيم تحتوي على هيدروكسيد السترونتيوم. هذه قادرة على الالتزام بقوة بالأسطح ذات الخصائص المعدنية ، ومقاومة للماء وتحمل التغيرات المفاجئة في درجة الحرارة.
بسبب ثباتها الفيزيائي والكيميائي الجيد ، يتم استخدام هذه الدهون كمواد تشحيم صناعية.
استقرار البلاستيك
الغالبية العظمى من المواد البلاستيكية عندما تتعرض لعوامل مناخية مثل الشمس والمطر والأكسجين الجوي ، وتعديل خصائصها وتدهورها.
بسبب مقاومته الكبيرة للماء ، يضاف هيدروكسيد السترونتيوم إلى هذه البوليمرات - أثناء مرحلة الاندماج - بمثابة عامل استقرار في صناعة المنتجات البلاستيكية لإطالة عمرها الإنتاجي.
تطبيقات أخرى
- في صناعة الطلاء ، يتم استخدامه كإضافة أساسية لتسريع عملية التجفيف في الدهانات التجارية والصناعية.
- يتم الحصول على أملاح السترونتيوم أو أيونات السترونتيوم من هيدروكسيد السترونتيوم وتستخدم كمواد خام لإنتاج المواد النارية.
مراجع
- ويكيبيديا. (بدون تاريخ). السترونتيوم هيدروكسيد. تم الاسترجاع من en.wikipedia.org
- بوب كيم. (بدون تاريخ). السترونتيوم هيدروكسيد. تم الاسترجاع من pubchem.ncbi.nlm.nih.gov
- Lambert، I. and Clever، H. L. (2013). هيدروكسيدات الأرض القلوية في المياه والمحاليل المائية. تم الاسترجاع من books.google.co.ve
- كريبس ، ر. (2006). تاريخ واستخدام العناصر الكيميائية لأرضنا: دليل مرجعي. تم الاسترجاع من books.google.co.ve
- هانيويل. (بدون تاريخ). السترونتيوم هيدروكسيد Octahydrate. تعافى من honeywell.com


