كبريتات الألومنيوم (Al2 (SO4) 3) هيكل ، يستخدم ، أنواع ، سمية
ال كبريتات الألومنيوم هو ملح الألومنيوم غير العضوي من صيغة Al2(SO4)3, التي عادة ما تظهر كمادة صلبة بيضاء مع بلورات لامعة. سوف يتأثر لون المركب بتركيزه من الحديد وأي شوائب أخرى. هناك نوعان رئيسيان من كبريتات الألومنيوم: A و B.
في الصورة السفلية ، تظهر بلورات بيضاء من كبريتات الألومنيوم المائي. يمكن ملاحظة عدم وجود ألوان بنية اللون تدل على وجود أيونات حديدية داخل الشبكة البلورية.

كبريتات الألومنيوم هي ملح قابل للذوبان بشدة في الماء ، ومن النادر أن نجده في شكله اللامائي. عادة ما يكون رطب في شكل ثماني كبريتات الألومنيوم2(SO4)3.18H2O] أو hexadecahydrate [Al2(SO4)3.16H2O].
وبالمثل ، يمكن أن تشكل أملاح مزدوجة مع البوتاسيوم ، ومع الأمونيوم ، والمركبات المعروفة باسم الشب. في جزء منه قد يكون هذا بسبب تقارب الماء داخل الهيدرات للاحتفاظ بأيونات أخرى إلى جانب الألومنيوم.
يمكن أن تتحلل كبريتات الألومنيوم عن طريق عمل الماء في هيدروكسيد الألومنيوم وحمض الكبريتيك. هذه الخاصية سمحت باستخدامها كمحميض للتربة.
وهو أيضًا مركب سام ، خاصة عن طريق ملامسته للبودرة. ومع ذلك ، فإنه يحتوي على ما لا نهاية من الاستخدامات والتطبيقات التي تنطلق من تنقية المياه عن طريق طريقة التخثر ، يحدث من خلال استخدامه في العديد من الصناعات ، حتى استخدامه مع الأهداف العلاجية.
مؤشر
- 1 هيكل
- 2 ما المقصود بـ (الاستخدامات)
- 2.1 تخثر أو تلبد الماء
- 2.2 استخدم كمورد للأحبار وفي إعداد الورق
- 2.3 الاستخدامات الصناعية
- 2.4 الاستخدامات الطبية والعلاجية
- 2.5 استخدامات أخرى
- 3 إنتاج كبريتات الألومنيوم
- 4 أنواع
- 5 السمية
- 6 المراجع
هيكل
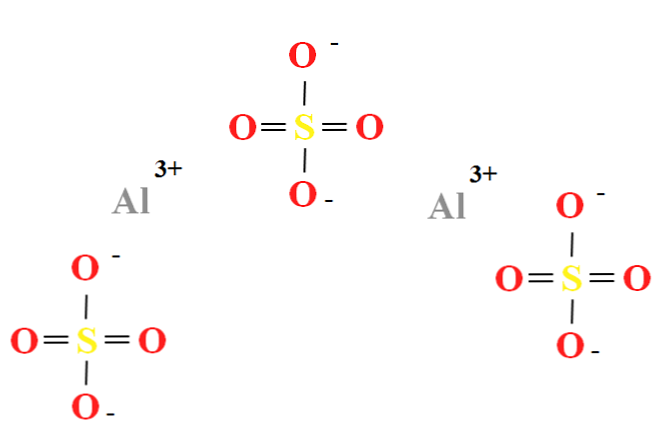
كبريتات الألومنيوم لديها نسبة الكاتيونات آل اثنين3+ لكل ثلاثة الأنيونات SO42- (الصورة العليا) ، والتي يمكن ملاحظتها مباشرة في صيغتها الكيميائية Al2(SO4)3.
لاحظ أن آل3+ هم رمادي ، في حين أن SO42- هم أصفر (لذرة الكبريت) والأحمر (لذرات الأكسجين).
الهيكل المصور يتوافق مع الشكل اللامائي لـ Al2(SO4)3, لأنه لا يوجد جزيء ماء يتفاعل مع الأيونات. في هيدراتك ، يمكن جذب الماء إلى المراكز الإيجابية لـ Al3+, أو من قبل SO رباعي الاسرة42- من خلال روابط الهيدروجين (HOH-O-SO32-).
ال2(SO4)3∙ 18 ساعة2أو ، على سبيل المثال ، يحتوي على 18 جزيء ماء في بنيته الصلبة. بعضهم قد يكون على اتصال مباشر مع آل3+ أو مع SO42-. بمعنى آخر: يمكن أن تحتوي كبريتات الألومنيوم على ماء تنسيق داخلي أو خارجي.
أيضا ، يمكن أن تستوعب هيكلها الكاتيونات الأخرى مثل الحديد3+, نا+, K+, إلخ ولكن لهذا ، فمن الضروري وجود المزيد من الأنيونات SO42-. لماذا؟ لتحييد الزيادة في الشحنات الإيجابية بسبب الشوائب المعدنية.
يمكن أن تحتوي كبريتات الألومنيوم على العديد من الهياكل ، على الرغم من أن هيدراتها تميل إلى اعتماد نظام بلوري أحادي.
الخصائص الفيزيائية والكيميائية
مظهر
يبدو كمادة صلبة مع بلورات بيضاء لامع ، حبيبات أو مسحوق.
الوزن الجزيئي
342.31 جم / مول (لا مائي).
رائحة
إنه عديم الرائحة
نكهة
طعم حلو قابض معتدل.
نقطة انصهار
770º م الشكل اللامائي (86.5 درجة مئوية أوكتاديكاهيدراتادا)
الذوبان في الماء
31.2 جم / 100 مل عند 0 درجة مئوية ؛ 36.4 جم / 100 مل عند 20 درجة مئوية و 89 جم / 100 مل على 100 درجة مئوية.
كثافة
2.67 إلى 2.71 جم / سم3.
الذوبانية
قابل للذوبان قليلاً في الكحول الإيثيلي.
ضغط البخار
أساسا الصفر.
استقرار
مستقرة في الهواء.
التحلل
عند تسخينها ، عند نقطة الانصهار تقريبًا ، يمكن أن تتحلل عن طريق إصدار أكسيد الكبريت ، وهو غاز سام على وجه الخصوص.
التآكل
حلول كبريتات الألومنيوم تآكل للألمنيوم. أيضا يمكن للمجمع تآكل المعادن في وجود الرطوبة.
الباكاف الحمضية
3.3 إلى 3.6. ودرجة الحموضة هو 2.9 أو أكثر في محلول مائي 5 ٪.
ما الغرض منه (الاستخدامات)
تخثر أو تلبد الماء
-عند مزجها بالماء (صالح للشرب ، خدم أو هدر) ، تسبب كبريتات الألمنيوم هيدروكسيد الألومنيوم ، الذي يشكل مجمعات مع المركبات والجزيئات في محلول تسريع ترسبها ، والتي في غياب المعالجة مع كبريتات الألومنيوم وقت طويل.
-تستخدم كبريتات الألومنيوم أيضًا في تنظيف مياه المسبح ، مما يجعلها أكثر جاذبية للاستخدام.
-من خلال استخدام كبريتات الألومنيوم ، يتم الحصول على المياه دون تعكر ولون ، مما يزيد من قدرتها على تسهيل تنظيف المياه. لسوء الحظ ، يمكن أن تؤدي طريقة التنقية هذه إلى زيادة تركيز الألومنيوم قليلاً في الماء.
-الألومنيوم هو معدن سام للغاية يتراكم في الجلد والدماغ والرئتين ، مما يسبب اضطرابات خطيرة. بالإضافة إلى ذلك ، لا يُعرف الوظيفة التي تؤديها في الكائنات الحية.
-يشترط الاتحاد الأوروبي ألا يتجاوز الحد الأقصى المسموح به للألمنيوم في الماء 0.2 مجم / لتر. وفي الوقت نفسه ، تتطلب وكالة حماية البيئة الأمريكية ألا يتجاوز الحد الأقصى لتلوث المياه بالألمنيوم من 0.05 إلى 2.2 ملغم / لتر.
-تتيح معالجة المياه العادمة أو المستخدمة مع كبريتات الألومنيوم التخلص من الفوسفور أو تقليله اقتصاديًا.
استخدم كمورد للأحبار وفي إعداد الورق
-لقد تم استخدام كبريتات الألومنيوم كأداة لفصل الأصباغ أو الأحبار ، مما يساعد على تثبيت المواد المراد صبغها. الإجراء الخاص بالتثبيت يرجع إلى Al (OH)3, الذي يساهم اتساق الجيلاتين في امتصاص الأصباغ على المنسوجات.
-على الرغم من أنه قد تم استخدامه منذ حوالي عام 2000 قبل الميلاد للغرض الموصوف ، إلا أن الأصباغ العضوية هي فقط التي تتطلب mordants. الأصباغ الاصطناعية ، من ناحية أخرى ، لا تتطلب mordants لأداء وظيفتها.
-لقد تم تهجيره من صناعة الورق ، لكنه لا يزال يستخدم في إنتاج لب الورق. يزيل الشوائب ، كما تم استخدامه لربط المواد وتحييد الشحنات ومعايرة الصنوبري.
الاستخدامات الصناعية
-يتم استخدامه في صناعة البناء من أجل تسريع وضع الخرسانة. بالإضافة إلى ذلك ، يتم استخدامه في تسرب المياه من المباني.
-في صناعة الصابون والدهون ، يتم استخدامه في إنتاج الجلسرين.
-يتم استخدامه في صناعة النفط في صناعة المحفزات الاصطناعية التي يتم استخدامها أثناء التشغيل.
-يتم استخدامه في صناعة الأدوية كعقولة في إعداد الأدوية ومستحضرات التجميل.
-يتدخل في إنتاج الأصباغ مثل القرمزي. كما أنها تستخدم صبغة في صناعة المطاط الصناعي من البيوتاديين ستايرين.
-في صناعة تصنيع السكر ، يتم استخدامه كتنقية دبس السكر.
-يتم استخدامه في صناعة مزيلات العرق. لماذا؟ لأنه يسبب تضييق قنوات الغدد العرقية ، وبالتالي الحد من تراكم العرق ، وهو وسيلة ضرورية لنمو البكتيريا التي تسبب الرائحة.
-يتم استخدامه في دباغة الجلود ، وهي العملية اللازمة لاستخدامه. بالإضافة إلى ذلك ، يتم استخدامه في صناعة الأسمدة.
-يتم استخدامه كمادة مضافة في إعداد الدهانات والمواد اللاصقة ومانعات التسرب ، وكذلك منتجات التنظيف والعناية بالأثاث..
الاستخدامات الطبية والعلاجية
-كبريتات الألومنيوم هي مادة مساعدة مناعية. لذلك ، فهي تفي بوظيفة معالجة المستضدات بطريقة تؤدي ، عند إطلاقها في موقع عملها ، إلى إنتاج أكبر للأجسام المضادة للمستضدات التي تم تلقيحها.
-إن المواد المساعدة لـ Freund و BCG ، وكذلك المواد المساعدة الأخرى ، بما في ذلك المواد الداخلية المنشأ مثل interleukins ، غير محددة لمستضدات ، مما يسمح بزيادة في نصف قطر الحركة المناعية. وقد أتاح ذلك تطوير لقاحات ضد العديد من الأمراض.
-أتاح تأثير التخثر لكبريتات الألومنيوم القضاء على العديد من الفيروسات في المياه المعالجة ، من بين أمور أخرى: Q beta و MS2 و T4 و P1. تشير النتائج إلى أن معالجة الماء بكبريتات الألمنيوم تؤدي إلى تعطيل هذه الفيروسات.
-يتم استخدام كبريتات الألومنيوم في شكل عصا أو كمسحوق في علاج الجروح أو التآكل السطحي الصغير الناتج عند الحلاقة.
-يستخدم في تصنيع أسيتات الألومنيوم ، وهو مركب يستخدم في علاج بعض حالات الأذن. كما تم استخدامه ، دون نجاح كبير ، لتخفيف عواقب لدغات النمل النار..
-يتم استخدام محاليل سلفات الألومنيوم بتركيز 5٪ إلى 10٪ في المعالجة المحلية للقرحة التي تسمح بالتحكم في إفرازاتها..
-يعمل الدواء القابض لكبريتات الألومنيوم على تقليص الطبقات السطحية للجلد ، وتخثر البروتينات وتضميد الجروح..
استخدامات أخرى
-تساعد كبريتات الألومنيوم في التحكم في النمو المفرط للطحالب في الأحواض والبحيرات وفي مجاري المياه. كما أنها تستخدم في إزالة الرخويات ، من بين أمور أخرى سبيكة إسبانية.
-يطبق البستانيون هذا المركب لتحمض التربة القلوية. عند ملامسة الماء ، تتحلل كبريتات الألومنيوم إلى هيدروكسيد الألومنيوم وحمض الكبريتيك المخفف. بعد ذلك ، يترسب هيدروكسيد الألومنيوم ، تاركًا حمض الكبريتيك في محلول.
-يتم تصور تحمض التربة الناجم عن حمض الكبريتيك بطريقة مبتكرة للغاية ، بسبب وجود نبات يسمى Hydrangea ، تتحول أزهاره إلى اللون الأزرق في وجود تربة حمضية ؛ أي أنها حساسة وتستجيب للتغيرات في درجة الحموضة.
-تشارك كبريتات الألومنيوم في إنتاج رغوة لمكافحة الحريق والسيطرة عليه. كيف؟ يتفاعل مع بيكربونات الصوديوم ، مما ينتج عنه إطلاق ثاني أكسيد الكربون2. هذا الغاز كتل وصول يا2 إلى موقع الاحتراق للمواد ؛ وبالتالي وقف إطلاق النار الذي كان يتطور.
إنتاج كبريتات الألومنيوم
يتم تصنيع كبريتات الألومنيوم عن طريق تفاعل مركب غني بالألمنيوم ، مثل خام البوكسيت ، مع حامض الكبريتيك في درجات حرارة مرتفعة. تمثل المعادلة الكيميائية التالية التفاعل:
ل2O3 + H2SW4 -> آل2(SO4)3 + 3 ساعات2O
يمكن أيضًا تشكيل كبريتات الألومنيوم عن طريق تفاعل تحييد بين هيدروكسيد الألومنيوم وحمض الكبريتيك ، وفقًا للتفاعل التالي:
2 آل (أوهايو)3 + 3 ساعات2SW4 + 12 ساعة2يا -> آل2(SO4)3.18H2O
يتفاعل حمض الكبريتيك مع الألومنيوم لتكوين كبريتات الأمونيوم وإطلاق جزيئات الهيدروجين في شكل غاز. رد فعل منظم على النحو التالي:
2 آل + 3 ساعات2SW4 -> آل2(SO4)3 + 3 ساعات2
نوع
تصنف كبريتات الألومنيوم إلى نوعين: النوع A والنوع B. في كبريتات الألومنيوم نوع A ، والمواد الصلبة بيضاء ولها تركيز حديد أقل من 0.5 ٪.
في كبريتات الألومنيوم من النوع B ، تكون المواد الصلبة بنية اللون ويبلغ تركيز الحديد فيها أقل من 1.5 ٪.
هناك صناعات تنتج كبريتات الألومنيوم التي لها معايير مختلفة لتصنيفها. وبالتالي ، تُبلغ الصناعة عن تحضيرها لكبريتات الألومنيوم من النوع A بتركيز أقصى يبلغ 0.1٪ من الحديد كأكسيد حديدي. بينما بالنسبة للنوع B ، فإنها تشير إلى تركيز حديدي أقصى يبلغ 0.35 ٪.
سمية
-كبريتات الألومنيوم هي مركب يمارس نشاطه السام عن طريق ملامسة غباره ، مما يسبب تهيج الجلد ، وفي الحالات التي يكون التلامس فيها متكررًا ، التهاب الجلد.
-في العين ، فإنه يسبب تهيجًا قويًا ، حتى ينتج عنه إصابات دائمة.
-استنشاق يسبب تهيج الأنف والحلق ، والتي يمكن أن تسبب السعال والطفح الجلدي.
-تناوله يسبب تهيج المعدة والغثيان والقيء.
-هناك تأثيرات سامة على الرغم من أنها ليست مباشرة بسبب كبريتات الألومنيوم ، إلا أنها غير مباشرة بسبب استخدامها. هذه هي حالة بعض الآثار السامة للألمنيوم ، الناجمة عن استخدام كبريتات الألومنيوم في تنقية المياه.
-يعاني المرضى الذين يتم غسيلهم لغسيل الكلى بشكل مزمن باستخدام أملاح محضرة في المياه النقية ، من خلال استخدام كبريتات الألومنيوم ، من اضطرابات صحية شديدة الشدة. بين هذه الاضطرابات لدينا فقر الدم والخرف عن طريق غسيل الكلى وزيادة في أمراض العظام.
مراجع
- ويكيبيديا. (2018). كبريتات الألومنيوم مأخوذة من: en.wikipedia.org
- آريس الصناعية محلول كبريتات الألومنيوم نوع A و B. مأخوذة من: aris.com.pe
- كريستوفر بويد (9 يونيو 2014). أهم الاستخدامات الصناعية لكبريتات الألومنيوم. مأخوذة من: chemservice.com
- بوب كيم. (2018). كبريتات الألومنيوم اللامائية. مأخوذة من: pubchem.ncbi.nlm.nih.gov
- أنديسيا الكيماويات (20 أغسطس 2009). ورقة السلامة من كبريتات الألومنيوم. [PDF]. مأخوذة من: andesia.com
- كتاب الكيميائية. (2017). كبريتات الألومنيوم. مأخوذة من: chemicalbook.com


