يستخدم كبريتيد الفضة (Ag2S) هيكل ، والخصائص ، والتسميات
ال كبريتيد الفضة هو مركب غير عضوي الصيغة الكيميائية هي Ag2S. يتكون من مادة صلبة سوداء اللون رمادية مكونة من الكاتيونات Ag+ والأنيونات S2- في نسبة 2: 1. ال2- انها مماثلة جدا ل Ag+, لأن كلاهما أيونات ناعمة ويمكنهما الاستقرار مع بعضهما البعض.
الحلي الفضية تميل إلى التغميق ، وتفقد بريقها المميز. تغيير اللون ليس نتاج أكسدة الفضة ، ولكن تفاعله مع كبريتيد الهيدروجين الموجود في البيئة بتركيزات منخفضة ؛ هذا يمكن أن يأتي من تعفن أو تدهور النباتات والحيوانات أو الأطعمة الغنية بالكبريت.

ح2يتفاعل S ، الذي يحمل جزيئه ذرة كبريت ، مع الفضة وفقًا للمعادلة الكيميائية التالية: 2Ag (s) + H2S (g) => Ag2S (ق) + ح2(G)
لذلك ، فإن Ag2S هي المسؤولة عن الطبقات السوداء التي تشكلت على الفضة. ومع ذلك ، في الطبيعة ، يمكن أيضًا العثور على هذا الكبريت في معادن الأسنتيتا والأرجنتين. يتميز المعدنان عن العديد من المعادن الأخرى ببلوراتها السوداء الساطعة ، مثل تلك الموجودة في الصورة الصلبة في الصورة العليا.
الآغ2تقدم S هياكل متعددة الأشكال ، خواص إلكترونية وضوئية جذابة ، وهي أشباه الموصلات ، وتعد بأن تكون مادة لتطوير الأجهزة الكهروضوئية ، مثل الخلايا الشمسية.
مؤشر
- 1 هيكل
- 2 خصائص
- 2.1 الوزن الجزيئي
- 2.2 المظهر
- 2.3 الرائحة
- 2.4 نقطة انصهار
- 2.5 الذوبان
- 2.6 هيكل
- 2.7 معامل الانكسار
- 2.8 ثابت عازل
- 2.9 الالكترونيات
- 2.10 رد فعل الحد
- 3 تسميات
- 3.1 علم اللاهوت النظامي
- 3.2 الأسهم
- 3.3 التقليدية
- 4 الاستخدامات
- 5 المراجع
هيكل
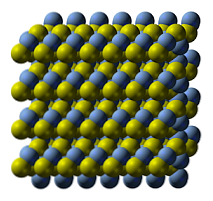
ويتضح الهيكل البلوري لكبريتيد الفضة في الصورة العليا. المجالات الزرقاء تتوافق مع الكاتيونات Ag+, في حين أن الأصفر إلى الأنيونات S2-. الآغ2S عبارة عن متعدد الأشكال ، مما يعني أنه يمكن أن يتبنى العديد من الأنظمة البلورية في ظل ظروف درجة حرارة معينة.
كيف؟ من خلال المرحلة الانتقالية. يتم إعادة ترتيب أيونات بطريقة لا تؤدي الزيادة في درجة الحرارة والاهتزازات الصلبة إلى إزعاج توازن الجذب الكهربائي. عندما يحدث هذا ، يقال أن هناك مرحلة انتقالية ، وبالتالي فإن المادة الصلبة تعرض خصائص مادية جديدة (مثل اللمعان واللون).
الآغ2S في درجات الحرارة العادية (أقل من 179 درجة مئوية) ، لديها بنية بلورية أحادية (α- Ag2S). إلى جانب هذه المرحلة الصلبة هناك مرحلتان أخريان: المكعب (المتمركز في الجسم) بين 179 إلى 586 درجة مئوية ، والمركب المكعب (المتمركز في الوجوه) عند درجات حرارة عالية جدًا (δ- Ag2S).
يتكون معدن الأرجنت من مرحلة fcc ، والتي تعرف أيضًا باسم β-Ag2S. بمجرد تبريده وتحويله إلى جرف ، تسود ميزاته الهيكلية مجتمعة. لذلك ، تتعايش كلاً من الهياكل البلورية: أحادي الطبقة ونسخة مخفية. وبالتالي ، تظهر مواد صلبة سوداء ذات ألوان مشرقة ومثيرة للاهتمام.
خصائص
الوزن الجزيئي
247.80 جم / مول
مظهر
بلورات سوداء رمادية
رائحة
مرحاض.
نقطة انصهار
836ºC. هذه القيمة تتفق مع حقيقة أن Ag2S مركب ذو طبيعة أيونية صغيرة ، وبالتالي يذوب في درجات حرارة تقل عن 1000 درجة مئوية.
الذوبانية
في الماء فقط 6.21 ∙ 10-15 غ / ل في 25 درجة مئوية. وهذا يعني أن كمية المادة الصلبة السوداء التي يتم ذوبانها ضئيلة. هذا ، مرة أخرى ، يرجع إلى الطابع القطبي الصغير للرابطة Ag-S ، حيث لا يوجد فرق كبير في النشاط الكهربائي بين الذرتين.
أيضا ، و Ag2S غير قابل للذوبان في جميع المذيبات. لا يوجد جزيء يمكنه فصل طبقاته البلورية بكفاءة في أيونات Ag+ و S2- الإذابة بالإكترونات.
هيكل
يمكن أيضًا رؤية أربع طبقات من روابط S-Ag-S في صورة الهيكل ، والتي تتحرك فوق بعضها البعض عندما تتعرض المادة الصلبة للفهم. هذا السلوك يعني أنه على الرغم من كونه أشباه الموصلات ، إلا أنه يدوم مثل كثير من المعادن في درجة حرارة الغرفة.
تتناسب طبقات S-Ag-S بشكل صحيح بسبب هندستها الزاوية التي يتم ملاحظتها على شكل متعرج. تتمتع هذه القوة بقوة الفهم ، وهي تتحرك على محور الإزاحة ، مما يؤدي إلى تفاعلات غير تساهمية جديدة بين ذرات الفضة والكبريت.
معامل الانكسار
2.2
ثابت عازل
6
إلكتروني
الآغ2S هو أشباه الموصلات ، أي أنه يتصرف كما لو كان من النوع ن ومن النوع ص. كما أنها ليست هشة ، لذلك تمت دراستها لتطبيقها في الأجهزة الإلكترونية.
رد فعل الحد
الآغ2يمكن اختزال S إلى الفضة المعدنية باستحمام القطع السوداء بالماء الساخن ، وهيدروكسيد الصوديوم ، والألمنيوم والملح. يحدث رد الفعل التالي:
3AG2S (s) + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2O3(S)
تسمية
الفضة ، التي التكوين الإلكتروني هو [كر] 4D105S1, يمكن أن يفقد إلكترونًا واحدًا فقط: ذلك الإلكترون في أقصى خمس مدارات له. وبالتالي ، فإن الكاتيون حج+ يبقى مع التكوين الإلكتروني [كر] 4D10. لذلك ، يحتوي على تكافؤ فريد لـ +1 ، والذي يحدد كيفية استدعاء مركباته.
الكبريت ، من ناحية أخرى ، لديه التكوين الإلكتروني [ني] 3s23P4, ويحتاج إلكترونين لإكمال ثمانيه التكافؤ. عندما يكسب هذين الإلكترونين (من الفضة) ، يتحول إلى أنيون الكبريت ، S2-, مع التكوين [ع]. وهذا هو ، فمن isoelectronic ليقول الغاز النبيل.
بحيث Ag2يجب استدعاء S وفقًا للتسميات التالية:
النظاميات
قردكبريتيد ديالفضة. هنا نعتبر عدد ذرات كل عنصر ويتم الإشارة إليها بواسطة بادئات البسط اليونانية.
الأوراق المالية
كبريتيد الفضة. عند وجود تكافؤ فريد لـ +1 ، لا يتم تحديده بالأرقام الرومانية بين قوسين: كبريتيد الفضة (I) ؛ هذا غير صحيح.
تقليدي
Sulfuro argéntمنظمة البن الدولية. نظرًا لأن الفضة "تعمل" بتكافؤ +1 ، تتم إضافة اللاحقة -ico إلى اسمها فضة في اللاتينية.
تطبيقات
بعض الاستخدامات الجديدة لـ Ag2S هي الآتية:
-تلوينات محاليل الجسيمات النانوية (بأحجام مختلفة) ، لها نشاط مضاد للجراثيم ، وليست سامة ، وبالتالي يمكن استخدامها في مجالات الطب وعلم الأحياء.
-يمكن أن تشكل الجسيمات النانوية ما يعرف بالنقاط الكمومية. هذه تمتص وتنبعث الإشعاع بكثافة أكبر من العديد من جزيئات الفلورسنت العضوية ، بحيث يمكن أن تحل محل الأخير كعلامات بيولوجية.
-هياكل α-Ag2S جعله يحمل الخصائص الإلكترونية ملفتة للنظر لاستخدامها كخلايا شمسية. كما أنه يمثل نقطة انطلاق لتوليف مواد وأجهزة استشعار حرارية جديدة.
مراجع
- مارك بيبلو. (17 أبريل 2018). كبريتيد الفضة أشباه الموصلات تمتد مثل المعادن. مأخوذة من: cen.acs.org
- التعاون: مؤلفي ومحرري البنية البلورية للكبريتيد الفضي (Ag2S) III / 17E-17F-41C (). In: Madelung O.، Rössler U.، Schulz M. (eds) Non-Tetrahedrally Bonded Elements and Binary Compounds I. Landolt-Börnstein - Group III Condensed Matter (Numerical Data and Functional Relationships in Science and Technology)، vol 41C. سبرينغر ، برلين ، هايدلبرغ.
- ويكيبيديا. (2018). كبريتيد الفضة. مأخوذة من: en.wikipedia.org
- ستانيسلاف إ. سادوفنيكوف. (يوليو 2016). حج2S جسيمات الفضة كبريتيد النانو والمحاليل الغروية: التوليف والخصائص. مأخوذة من: sciencedirect.com
- مواد آزو. (2018). كبريتيد الفضة (Ag2S) أشباه الموصلات. مأخوذة من: azom.com
- إيه. نوف. (2015). آفاق وتحديات الأفلام الرقيقة من كبريتيد الفضة: مراجعة. قسم علوم المواد والطاقة المتجددة ، قسم الفيزياء الصناعية ، جامعة ولاية إبوني ، أباكاليكي ، نيجيريا.
- UMassAmherst. (2011). محاضرات توضيحية: تنظيف الفضة المشوهة. مأخوذة من: lecturedemos.chem.umass.edu
- الدراسة. (2018). ما هو كبريتيد الفضة؟ - الصيغة الكيميائية والاستخدامات. مأخوذة من: study.com


