غرام وصمة عار الأساس والمواد والتقنية والاستخدامات
ال غرام وصمة عار هي تقنية التلطيخ الأبسط والأكثر فائدة في علم الأحياء الدقيقة التشخيصي. تم إنشاء هذه التقنية من قبل الطبيب الدنماركي هانز كريستيان غرام في عام 1884 ، والذي تمكن من تصنيف البكتيريا في غرام إيجابية وسلبية الجرام ، وفقا لتكوين جدار الخلية.
خضعت التقنية لبعض التعديلات من قبل Hucker في عام 1921 لتحقيق الاستقرار في الكواشف وتحسين جودة وصمة عار ، بحيث يعرف Gain-stain أيضًا باسم Gram-Hucker.
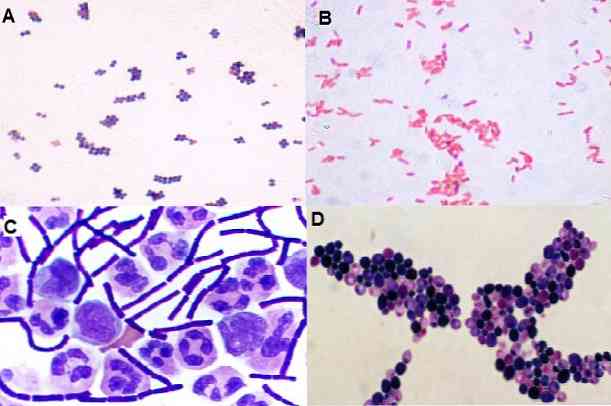
من خلال هذه التقنية ، من الممكن أيضًا ملاحظة الشكل الذي تتواجد به الكائنات الحية الدقيقة ، أي ما إذا كانت هذه المكورات هي العصعص ، العصيّات ، العصعص ، الأشكال المتعددة ، الخيطية ، وغيرها. وكذلك توزيعها في الفضاء: في الكتلة ، في السلسلة ، معزولة ، في أزواج ، في tetrads ، الخ.
عند الاشتباه في وجود عدوى بكتيرية ، ينبغي نشر معظم العينات المستلمة على شريحة وملطخة بالجرام لفحصها تحت المجهر..
سيرشد تقرير الجرام الطبيب إلى أي نوع من الكائنات الحية الدقيقة يمكن أن يكون سبب العدوى ، قبل الحصول على النتيجة النهائية للمحصول..
في بعض الحالات ، تكون حياة المريض شديدة الخطورة ، لذلك يحتاج الأطباء بشكل عاجل إلى تقرير غرام لإجراء علاج تجريبي ، في انتظار تحديد هوية الكائنات الحية الدقيقة.
على سبيل المثال ، إذا كشف الجرام عن وجود متلازمة موجبة للجرام في السائل النخاعي ، فإن الطبيب سيوجه العلاج الأولي بالمضادات الحيوية التي تقضي على هذا النوع من البكتيريا ، وفقًا للبروتوكولات الموضوعة له..
بمجرد وصول النتيجة النهائية باسم الكائنات الحية الدقيقة المعزولة والمضادات الحيوية الخاصة بها ، سيقوم الطبيب بتقييم ما إذا كان يجب تغيير العلاج أم لا. سيتم اتخاذ هذا القرار وفقًا لدراسة مدى حساسية الكائنات الحية الدقيقة للمضادات الحيوية التي تتلقاها وتطور المريض.
مؤشر
- 1 مؤسسة
- 2 المواد
- 3 إعداد الأصباغ والكواشف
- 3.1 حل الكريستال البنفسجي
- 3.2 Iodo-Lugol
- 3.3 التبييض
- 3.4 التباين
- 4 تخزين الكواشف
- 5 تحضير انتشار العينة لتكون ملونة
- 5.1 غرام من العينات المباشرة
- 5.2 غرام من المحاصيل
- 6 تقنية
- 7 فائدة
- 8 الأخطاء الشائعة
- 9 المراجع
مؤسسة
هذا هو الأسلوب الذي يقدم 4 خطوات أساسية: تلطيخ ، والتثبيت مع mordant ، تلون و contratinction. لذلك ، هذه التقنية بالإضافة إلى تلوين البكتيريا ، تميزها أيضًا.
البنفسجي الكريستال هو أول تلوين المستخدمة. لديها تقارب للببتيدوغليكان والأرجواني سوف تلطيخ جميع البكتيريا الموجودة ، ثم يتم وضع اللوغول ، الذي يعمل كدليل ، أي أنه سيحث على تكوين مجمعات غير قابلة للذوبان من بروتينات اليود البنفسجية البلورية - داخل الخلية النووية..
تشكل البكتيريا الموجبة للجرام ، والتي تحتوي على جدار سميك من الببتيدوغليكان ، المزيد من المركبات (البلورات البنفسجية - اليود) ، وبالتالي فإنها تحتفظ بالصبغة.
كما أنه يؤثر على أن جدار البكتيريا إيجابية الجرام يحتوي على كمية أكبر من الأحماض غير المشبعة ، والتي تظهر تقارب عالٍ للعوامل المؤكسدة (Lugol).
وفي الوقت نفسه ، تحتوي البكتيريا سالبة الجرام على طبقة رقيقة من الببتيدوغليكان ، مما يجعل البكتيريا أقل تعقيدًا من البكتيريا إيجابية الجرام..
ثم تأتي خطوة تلون ، حيث تتصرف البكتيريا إيجابية الجرام وسالبة الجرام بشكل مختلف.
تحتوي البكتيريا السالبة للجرام على غشاء خارجي غني بسكريات الدهون الشحمية التي تشكل جزءًا من جدارها الخلوي. يتم تدمير الدهون عن طريق ملامسة أسيتون الكحول ، وبالتالي فإن الغشاء الخارجي مزعزع للاستقرار ، ويتم إطلاق البلورة البنفسجية.
هذه هي الطريقة التي يتم بها تلويثها بالسافران أو الفوشين الأساسي ، مع أخذ اللون الأحمر.
في حالة البكتيريا إيجابية الجرام ، فإنها تقاوم تغير اللون لأن التبييض يعمل على إغلاق المسام ، مما يمنع مركب البنفسج / اليود من الهروب.
لذلك ، فإن التلوين مع الكريستال البنفسجي مستقر ، وليس هناك مجال للسافران أو الفوشين. وبسبب هذا ، هذه البكتيريا وصمة عار شديدة اللون الأزرق أو الأرجواني.
المواد
تتكون مجموعة تلوين غرام من:
- الكريستال البنفسجي
- وغول
- الكحول الأسيتون
- Safranin أو fuchsin الأساسية
تحضير الأصباغ والكواشف
حل الكريستال البنفسجي
الحل أ:
الكريستال البنفسجي -2 غرام
الكحول الإيثيلي 95 ٪ -20cc
الحل ب:
أكسالات الأمونيوم -0.8 غرام
الماء المقطر -80 سم مكعب
من أجل التحضير النهائي لبلورة البنفسج ، يجب تخفيف محلول 01:10 بالماء المقطر وخلطه مع 4 أجزاء من المحلول B. يتم تخزين الخليط لمدة 24 ساعة قبل الاستخدام. يتم ترشيحه في قارورة لتلطيخ العنبر باستخدام مرشح ورق.
يتم نقل المبلغ الذي سيتم استخدامه يوميًا إلى قنينة العنبر مع قطارة.
يودو-غول
وزن وقياس الكمية المشار إليها من كل مركب ، على النحو التالي:
بلورات Iodo - 1gr
يوديد البوتاسيوم - 2 غرام
الماء المقطر -300 سم مكعب
يذوب يوديد البوتاسيوم شيئًا فشيئًا في الماء ثم يضاف اليود. حلق الحل لزجاجة العنبر الملونة.
يتم نقل المبلغ الذي سيتم استخدامه يوميًا إلى زجاجة كهرماني أصغر مع قطارة.
تبيض
95 ٪ الكحول الإيثيلي -50 مل
الأسيتون - 50 مل
وهي مستعدة في أجزاء متساوية. تغطية جيدا ، فإنه يميل إلى تتبخر.
ضع في زجاجة مع قطارة.
يوفر هذا المستحضر تلونًا في الوقت المعتدل من 5 إلى 10 ثوانٍ وهو الأكثر الموصى به.
يفضل المبتدئين استخدام الكحول الإيثيلي بنسبة 95٪ فقط ، حيث يكون اللون أبطأ من 10 إلى 30 ثانية.
في حين أن الأكثر خبرة يمكنهم استخدام الأسيتون النقي ، حيث يحدث تغير اللون بسرعة كبيرة من 1 إلى 5 ثوانٍ.
تباين
سافران الأسهم الحل
Safranina -2.5 غرام
الكحول الإيثيلي 95 ٪ -100 سم مكعب
بعد وزن الكمية المذكورة من سافران يذوب في 100 سم مكعب من الكحول الإيثيلي إلى 95 ٪.
يتم إعداد حل safranin العامل من محلول المخزون.
للقيام بذلك ، وقياس 10 سم مكعب من محلول المخزون ، إضافة 90 سم مكعب من الماء المقطر لإكمال 100 مل.
يوصى بنقل الكمية التي سيتم استخدامها يوميًا في زجاجة العنبر مع قطارة.
الكائنات الحية الدقيقة التي تلطخ بشكل ضعيف سلبية الجرام مع وصمة الجرام هوكر ، مثل بعض اللاهوائية, Legionella sp و Campylobacter sp و Brucella sp, يمكن أن تكون ملطخة بشكل أفضل إذا تم استخدام التعديل الذي أجراه Kopeloff على تلطيخ Gram-Hucker ، والمسمى Gram-Kopeloff stain ،.
هذه التقنية تغير صبغة سافران بواسطة fuchsin الأساسية. مع هذا التعديل ، يمكن تلوين الكائنات الحية الدقيقة المذكورة أعلاه بفعالية.
تخزين الكواشف
يجب تخزين الأصباغ المعدة في درجة حرارة الغرفة.
إعداد عينة تنتشر إلى اللون
يجب أن تحتوي العينة على 10 على الأقل5 الكائنات الحية الدقيقة قبل مراقبة الكائنات الحية الدقيقة في اللطاخة من المرجح. يمكن أن ينتشر من عينة مباشرة أو الثقافات في وسائل الإعلام الصلبة أو السائلة.
يجب أن تكون الفروق موحدة وموزعة بشكل جيد وليست سميكة للغاية ، من أجل رؤية أفضل للهياكل الموجودة.
-غرام من العينات المباشرة
البول غرام دون أجهزة الطرد المركزي
يتم خلط البول ويتم وضع 10 ميكرولتر على شريحة. تشير ملاحظة حقل بكتيريا / غمر واحد على الأقل إلى وجود عدوى.
هذا يعني أن الثقافة سوف تحتوي على أكثر من 100،000 CFU / مل (105 CFU / مل) من البول في 85 ٪ من الحالات.
هذه الطريقة ليست مفيدة لتعدادات المستعمرة التي تقل عن 100،000 CFU.
LCR غرام
يجب أن يكون الطرد المركزي CSF ، وإزالة طاف وانتشار بيليه على شريحة. هذا السائل معقم في الظروف العادية. ملاحظة البكتيريا تشير إلى العدوى.
غرام من عينات الجهاز التنفسي
إن الغشاء البلغم أو غسل الشعب الهوائية أو القصبات السنوية ، رغم أنه قد يكون هناك مجموعة متنوعة من الكائنات الحية الدقيقة ، سوف يوجه دائمًا في التشخيص ، إلى جانب كونه مفيدًا لنوع الخلايا التي تمت ملاحظتها.
في حالة البلغم ، يجب تحضير اللطاخ مع الأجزاء الأكثر صرامة من العينة.
البراز غرام
لا ينصح بإجراء غرام لهذا النوع من العينات ، لأنه ليس له قيمة تشخيصية.
-محاصيل الجرام
يمكن القيام به بطريقتين ، واحدة من المحاصيل السائلة والآخر من المحاصيل الصلبة.
المحاصيل السائلة
من الثقافات السائلة أنها بسيطة للغاية. تحت أخف وزنا تؤخذ العديد من المحمص من مرق عكر وتوضع على شريحة نظيفة وجافة ، وإعطاء حركات دائرية من المركز نحو المحيط ، لتوزيع المواد بشكل موحد.
يسمح ليجف تلقائيا في الهواء. مرة واحدة جافة ، يتم إصلاح المواد إلى ورقة مع الحرارة. لهذا ، بمساعدة المشبك ، يتم تمرير الورقة 3 4 مرات عبر لهب الموقد بنسن ، مع الحرص على عدم حرق المواد.
يسمح للورقة بالتبريد ووضعها على جسر التلوين.
المحاصيل الصلبة
لتنفيذ امتداد لصبغة غرام من ثقافة صلبة ، تابع ما يلي:
قبل اختيار المستعمرات الواجب اتخاذها ، يجب إعداد الشريحة ، ووضع قطرتين تقريبًا من محلول ملحي فسيولوجي معقم.
إذا كانت لوحة الثقافة الأصلية تحتوي على عدة أنواع مختلفة من المستعمرات ، فسيتم اختيار مستعمرة معزولة من كل واحدة لأداء الغرام. سيتم أخذ كل مستعمرة مع الحلقة البلاتينية لحلها في محلول ملحي سبق وضعها على الشريحة.
يتم إعطاء حركات دائرية من المركز إلى المحيط ، لتوزيع مستعمرة متجانسة على الشريحة..
يسمح ليجف تلقائيا في الهواء. بمجرد أن يتم تجفيف الطبقة بالحرارة ، كما هو موضح أعلاه (إحراق الشريحة بأفتح) ، احرص على عدم حرق المواد.
يجب تنفيذ هذا الإجراء مع كل نوع مختلف من المستعمرات. على قطعة من الورق يجب ملاحظة ترتيب الملاحظة ، على سبيل المثال:
مستعمرة 1: مستعمرة انحلالية للبيتا الصفراء: لوحظت الكسي إيجابية الغرام في التجمعات
مستعمرة 2: مستعمرة الكريمة ، بدون انحلال الدم: لوحظ وجود عصيات سلبية الغرام.
يجب تسمية كل ورقة لمعرفة ما نلاحظه.
تقنية
تقنية تلطيخ الجرام بسيطة للغاية في الأداء وغير مكلفة نسبيًا ولا يمكن تفويتها في أحد مختبرات الأحياء الدقيقة.
ويتم ذلك على النحو التالي:
- ثبت اللطاخة بالحرارة ثم ضعها على الجسر الملون.
- الورقة مغطاة بالكامل بزجاج بنفسجي لمدة 1 دقيقة.
- تغسل بالماء. لا تجف
- غطي الطبق بمحلول Lugol ، واتركه لمدة دقيقة واحدة. تغسل بالماء. لا تجف.
- امزج لمدة 5-10 ثوان مع التحريض اللطيف في كحول الأسيتون. أو ضع الورقة في وضع مستقيم وإسقاط قطرات من وكيل إزالة اللون على السطح حتى يتم سحب الزجاج البنفسجي المتبقية بعيدا. لا تتجاوز.
- تغسل بالماء. لا تجف.
- استبدل الورقة الموجودة على الجسر الملون والغطاء لمدة 30 ثانية بالسافران (Gram-Hucker) أو دقيقة واحدة باستخدام fuchsin الأساسي (Gram-Kopeloff).
- تغسل بالماء
- السماح ليجف تلقائيا في الهواء الرأسي.
بمجرد أن تجف ، ضع قطرة واحدة من زيت الغمر لمراقبة ذلك تحت هدف 100X في المجهر الضوئي.
فائدة
هذه التقنية تسمح للتمييز بين الاختلافات الشكلية لمعظم البكتيريا.
تتميز الخمائر أيضًا بهذا اللون. يأخذون اللون البنفسجي البلّوري ، أي أنهم صبغة الجرام إيجابية.
من ناحية أخرى ، يمكن تمييز عصيّات الجراثيم الإيجابية الجرام ، حيث تُلاحظ مساحة واضحة داخل العصية ، حيث تم تشكيل البقعة الداخلية ، على الرغم من أن البوغات لا تلطخ جيدًا. لاستخدام الجراثيم ، يتم استخدام تقنيات أخرى مثل Shaeffer-Fulton.
تجدر الإشارة إلى أن هذه البقعة لا تعمل على تلوين جميع أنواع البكتيريا ، أي أن هناك حالات لا يعمل فيها التلوين..
في هذه الحالة ، يمكن ذكر البكتيريا التي تفتقر إلى جدار الخلية. على سبيل المثال: جنس الميكوبلازما ، البلازما الكروية ، يوريبلازما ، L- الأشكال والبروتوبلاست.
كما أنها تلطخ البكتيريا بشدة بجدران غنية بالأحماض الفطرية ، مثل المتفطرات والبكتيريا داخل الخلايا مثل الكلاميديا والريكتسياس.
كما أنه غير فعال في وصمة عار معظم البكتيريا spirochetal.
هناك بكتيريا من نفس الجنس يمكن ملاحظتها في نفس العينة مثل الجرام موجبة والسالبة للجرام. عندما يحدث هذا يطلق عليه متغير جرام وصمة عار ، والتي قد تكون راجعة إلى تغيير في العناصر الغذائية ، ودرجة الحرارة ، ودرجة الحموضة أو تركيز الشوارد..
الأخطاء الشائعة
التبييض بشكل مفرط
المبالغة في خطوة تلون يمكن أن يسبب مراقبة الكائنات الحية الدقيقة سلبية الغرام زائفة.
لا تنتظر وقت التجفيف الكافي لإضافة زيت الغمر:
هذا الخطأ يتسبب في تكوين micelles الدهنية التي تجعل من الصعب مراقبة الهياكل الموجودة. يحدث هذا عندما ينضم الزيت إلى جزيئات الماء الموجودة في اللطاخة.
عكس ترتيب الكواشف:
خطأ مثل هذا سيؤدي إلى ظهور البكتيريا سالبة الجرام باللون الأرجواني ، أي إيجابية الجرام كاذبة.
استخدم المحاصيل القديمة (الصلبة أو السائلة):
يمكن أن يسبب البكتيريا إيجابية الجرام لصمة سلبية الجرام (سلبية الغرام سلبية). يحدث هذا لأنه في الثقافات القديمة من المحتمل وجود بكتيريا ميتة أو متدهورة وفي ظل هذه الظروف لا تحتفظ البكتيريا بلورة البنفسج.
استخدم حل Lugol القديم جدًا:
بمرور الوقت يفقد اللوغول خصائصه ويتلاشى لونه. إذا تم استخدام الكاشف المنحل بالفعل ، فلن يعمل على إصلاح اللون البنفسجي بشكل جيد ، وبالتالي هناك إمكانية للحصول على تصور للكائنات الحية الزائفة سالبة الجرام.
خلفية مزرق
خلفية ملونة بشكل صحيح ستكون حمراء. تشير الخلفية الزرقاء إلى أن اللون غير كافٍ.
مراجع
- ريان ك. ج. ، راي سي 2010. sherris. علم الاحياء المجهري Medical، 6th edition McGraw-Hill ، نيويورك ، الولايات المتحدة الأمريكية
- Koneman E، Allen S، Janda W، Schreckenberger P، Winn W. (2004). التشخيص الميكروبيولوجي. (الطبعة الخامسة). الأرجنتين ، التحرير البنميريكانا إس..
- Forbes B، Sahm D، Weissfeld A. 2009. Microbiological diagnosis of Bailey & Scott. 12 إد. الأرجنتين. Panamericana S.A Editorial
- Casas-Rincón G. 1994. Mycology General. 2nd Ed. Universidad Central de Venezuela، إصدارات المكتبة. فنزويلا ، كاراكاس.
- "غرام وصمة عار" ويكيبيديا ، الموسوعة الحرة. 4 أكتوبر 2018 ، 23:40 بالتوقيت العالمي. 9 ديسمبر 2018 ، 17:11. مأخوذة من es.wikipedia.org.
- González M ، González N. 2011. دليل علم الأحياء الدقيقة الطبي. الإصدار الثاني ، فنزويلا: مديرية الإعلام والمنشورات بجامعة كارابوبو.
- López-Jácome L، Hernández-Durán M، Colín-Castro C، Ortega-Peña S، Cerón-González G، Franco-Cendejas F. تلطيخ أساسي في مختبر الأحياء الدقيقة. بحث عن الإعاقة. 2014؛ 3 (1): 10-18.


