خصائص أنهيدريد ، كيف يتم تشكيلها ، تسميات ، تطبيقات
ال انهيدريدات هي مركبات كيميائية تنشأ من اتحاد جزيئين من خلال إطلاق الماء. وبالتالي ، يمكن أن ينظر إليه باعتباره الجفاف من المواد الأولية. على الرغم من أنه ليس صحيحا بالضبط.
في الكيمياء العضوية وغير العضوية يتم ذكرها ، وفي كلا الفرعين يختلف فهمها إلى حد كبير. على سبيل المثال ، في الكيمياء غير العضوية ، تعتبر الأكاسيد الأساسية والحمضية بمثابة أنهيدريدات من هيدروكسيداتها وأحماضها على التوالي ، حيث تتفاعل الأولى مع الماء لتكوين الأخير..

هنا يمكن أن يحدث ارتباك بين المصطلحين "اللامائي" و "أنهيدريد". بشكل عام ، يشير اللامائي إلى مركب تم تجفيفه دون حدوث تغييرات في طبيعته الكيميائية (بدون تفاعل) ؛ بينما مع أنهيدريد ، هناك تغيير كيميائي ، ينعكس في التركيب الجزيئي.
إذا تمت مقارنة الهيدروكسيدات والأحماض مع أكاسيدها المقابلة (أو أنهيدريد) ، فسيتم ملاحظة وجود تفاعل. في المقابل ، قد يتم ترطيب بعض الأكاسيد أو الأملاح ، وفقدان الماء ، وتبقى المركبات نفسها ؛ ولكن ، بدون ماء ، هذا لا مائي.
في الكيمياء العضوية ، من ناحية أخرى ، فإن المقصود من أنهيدريد هو التعريف الأولي. على سبيل المثال ، أحد أكثر الأنهيدريدات المعروفة هي مشتقات الأحماض الكربوكسيلية (الصورة العليا). هذه تتكون من اتحاد مجموعتي أسيل (-CO) عن طريق ذرة الأكسجين.
يشار في هيكلها العام R1 لمجموعة أسيل ، ور2 لمجموعة الأسيل الثانية. لأن ر1 و R2 أنها مختلفة ، أنها تأتي من الأحماض الكربوكسيلية المختلفة ، ثم أنهيدريد الحمض غير المتماثل. عندما يكون كل من بدائل R (سواء كانت عطرية أم لا) متماثلان ، فإننا نتحدث في هذه الحالة عن أنهيدريد الحمض المتماثل.
في وقت ربط اثنين من الأحماض الكربوكسيلية لتشكيل الأنهيدريد ، قد يتشكل الماء أو لا يتشكل ، وكذلك المركبات الأخرى. كل شيء يعتمد على هيكل الأحماض المذكورة.
مؤشر
- 1 خصائص أنهيدريد
- 1.1 التفاعلات الكيميائية
- 2 كيف تتشكل الأنهيدريدات?
- 2.1 أنهيدريد دوري
- 3 تسميات
- 4 تطبيقات
- 4.1 أنهيدريد عضوي
- 5 أمثلة
- 5.1 انهيدريد السكسينيك
- 5.2 أنهيدريد الجلوتاري
- 6 المراجع
خواص الانهيدريد
تعتمد خصائص أنهيدريد على ما تشير إليه. جميعها تقريبًا تشترك في تفاعلها مع الماء. ومع ذلك ، بالنسبة لما يسمى أنهيدريدات أساسية غير عضوية ، فإن العديد منها في الواقع غير قابل للذوبان في الماء (MgO) ، لذلك سوف يركز هذا البيان على أنهيدريدات الأحماض الكربوكسيلية.
تقع نقاط الانصهار والغليان على التركيب الجزيئي والتفاعلات بين الجزيئات لـ (RCO)2أو ، هذه هي الصيغة الكيميائية العامة لهذه المركبات العضوية.
إذا كانت الكتلة الجزيئية لـ (RCO)2أو أنها منخفضة ، فمن المحتمل أنها سائل عديم اللون في درجة حرارة الغرفة والضغط. على سبيل المثال ، أنهيدريد الخل (أو أنهيدريد الإيثانوي) ، (CH3CO)2أو أنها سائلة وذات أهمية صناعية أكبر ، كونها كبيرة للغاية في إنتاجها.
يمثل التفاعل بين أنهيدريد الخل والماء بالمعادلة الكيميائية التالية:
(CH3CO)2يا + ح2يا => 2CH3COOH
لاحظ أنه عند إضافة جزيء الماء ، يتم إطلاق جزيئين من حمض الأسيتيك. رد الفعل العكسي ، ومع ذلك ، لا يمكن أن يحدث لحمض الخليك:
2CH3COOH => (CH3CO)2يا + ح2يا (لا يحدث)
من الضروري اللجوء إلى طريق اصطناعي آخر. من ناحية أخرى ، يمكن للأحماض ثنائية الكربوكسيل القيام بذلك عن طريق التسخين ؛ ولكن سيتم شرحه في القسم التالي.
التفاعلات الكيميائية
تحليل بالماء
واحدة من أبسط تفاعلات أنهيدريد هو التحلل المائي ، الذي تم عرضه للتو بالنسبة لخليك أنهيدريد. بالإضافة إلى هذا المثال ، لدينا أنهيدريد حمض الكبريتيك:
H2S2O7 + H2O <=> 2H2SW4
هنا لديك أنهيدريد حمض غير عضوي. لاحظ أن ل H2S2O7 (ويسمى أيضًا حمض الكبريتيك) ، يكون رد الفعل نفسه قابلاً للانعكاس ، لذلك تسخين H2SW4 التركيز النتائج في تشكيل أنهيدريد لها. إذا كان ، من ناحية أخرى ، حل مخفف لـ H2SW4, يتم تحريرها SO3, أنهيدريد الكبريتيك.
الأسترة
يتفاعل أنهيدريد الحمض مع الكحول ، مع بيريدين في الوسط ، لإعطاء إستر وحمض كربوكسيلي. على سبيل المثال ، يعتبر التفاعل بين أنهيدريد الخل والإيثانول:
(CH3CO)2يا + CH3CH2OH => CH3CO2CH2CH3 + CH3COOH
وبالتالي تشكيل إيثيل استر إيثانوات ، CH3CO2CH2CH3, وحمض الإيثانويك (حمض الخليك).
عملياً ، ما يحدث هو استبدال هيدروجين مجموعة الهيدروكسيل بمجموعة أسيل:
R1-OH => R1-OCOR2
في حالة (CH3CO)2أو ، مجموعة أسيل الخاصة بك هي -COCH3. لذلك ، يقال أن مجموعة OH تعاني من الأكياس. ومع ذلك ، فإن الاسييل والإستري ليسا مفاهيم قابلة للتبادل. يمكن أن يحدث Acylation مباشرة في حلقة عطرية ، والمعروفة باسم acylation Friedel-Crafts.
وبالتالي ، يتم استنباط الكحول في وجود أنهيدريد الحمض بواسطة الأسيل.
من ناحية أخرى ، تتفاعل مجموعة واحدة فقط من مجموعتي الأسيل مع الكحول ، وتبقى الأخرى مع الهيدروجين الذي يتكون من حمض الكربوكسيل ؛ هذا بالنسبة لحالة (CH3CO)2أو إنه حمض الإيثانويك.
amidation
تتفاعل أنهيدريد الحمض مع الأمونيا أو مع الأمينات (الأولية والثانوية) لإعطاء الأميدات. رد الفعل مشابه جدا للاسترة الموصوفة للتو ، ولكن يتم استبدال ROH بأمين. على سبيل المثال ، أمين ثانوي ، R2NH.
مرة أخرى ، رد الفعل بين (CH3CO)2يا وديثيل أمين ، إلخ2NH:
(CH3CO)2يا + 2Et2NH => CH3كونيت2 + CH3COO-+NH2وآخرون2
و diethylacetamide ، تتشكل CH3كونيت2, وملح الأمونيوم كربوكسيلي ، CH3COO-+NH2وآخرون2.
على الرغم من أن المعادلة قد تبدو صعبة بعض الشيء لفهمها ، إلا أنه يكفي ملاحظة كيف قامت المجموعة -COCH3 يستعاض عن حاء2NH لتشكيل أميد:
وآخرون2NH => Et2NCOCH3
أكثر من مجرد وسط ، رد الفعل لا يزال أسيل. يتم تلخيص كل شيء في تلك الكلمة. هذه المرة ، يعاني الأمين من الأكياس وليس الكحول.
كيف يتم تشكيل أنهيدريد?
تتشكل أنهيدريدات غير عضوية من خلال تفاعل العنصر مع الأكسجين. وبالتالي ، إذا كان العنصر معدنيًا ، يتم تشكيل أكسيد الفلز الأساسي أو أنهيدريد ؛ وإذا كان غير معدني ، يتم تكوين أكسيد غير معدني أو أنهيدريد حامض.
بالنسبة للأنهيدريدات العضوية ، يكون رد الفعل مختلفًا. لا يمكن ربط اثنين من الأحماض الكربوكسيلية مباشرة بتحرير الماء وتشكيل أنهيدريد الحمض ؛ مطلوب مشاركة مركب لم يتم ذكره بعد: كلوريد الأسيل ، RCOCl.
يتفاعل حمض الكربوكسيل مع كلوريد الأسيل ، وينتج كل من أنهيدريد وكلوريد الهيدروجين:
R1COCl + R2COOH => (R1CO) يا (كور2) + حمض الهيدروكلوريك
CH3COCl + CH3COOH => (CH3CO)2يا + حمض الهيدروكلوريك
و CH3 يأتي من مجموعة الأسيتيل ، CH3ثاني أكسيد الكربون ، والآخر موجود بالفعل في حمض الخليك. يمكن أن يؤدي اختيار كلوريد أسيل معين ، وكذلك حمض الكربوكسيل ، إلى تخليق أنهيدريد الحمض المتماثل أو غير المتماثل.
أنهيدريد دوري
على عكس الأحماض الكربوكسيلية الأخرى التي تتطلب كلوريد الأسيل ، يمكن تكثيف الأحماض الكربوكسيلية في أنهيدريد المقابل. لهذا ، من الضروري تسخينها لتعزيز إطلاق H2على سبيل المثال ، يظهر تشكيل أنهيدريد الفثاليك من حمض الفثاليك.

لاحظ كيفية اكتمال الحلقة الخماسية ، والأكسجين الذي يربط كلا المجموعتين C = O هو جزء منه ؛ هذا هو أنهيدريد دوري. أيضا ، يمكن ملاحظة أن أنهيدريد الفثاليك هو أنهيدريد متماثل ، لأن كلا R1 كما R2 إنها متطابقة: حلقة عطرية.
ليست كل الأحماض ثنائية الكربوكسيل قادرة على تشكيل أنهيدريد ، لأنه عندما يتم فصل مجموعات COOH الخاصة بها على نطاق واسع ، فإنها تضطر إلى إكمال حلقات أكبر وأكبر. أكبر حلقة يمكن تشكيلها هي حلقة سداسية ، أكبر من أن رد الفعل لا يحدث.
تسمية
كيف يتم تسمية الانهيدريد؟ وإذا تركنا جانبا المواد غير العضوية المرتبطة بالأكسيدات ، فإن أسماء الأنهيدريدات العضوية الموضحة حتى الآن تعتمد على هوية R1 و R2. وهذا هو ، من مجموعات أسيل لها.
إذا كانت R's هي نفسها ، يكفي استبدال كلمة "acid" بكلمة "anhydride" في الاسم الخاص بحمض carboxylic. وإذا كان الأمر مختلفًا ، على النقيض من ذلك ، فإن Rs مختلفان ، يتم تسميتهما بترتيب أبجدي. لذلك ، لمعرفة ما يمكن تسميته ، من الضروري أولاً معرفة ما إذا كان أنهيدريد الحمض المتماثل أو غير المتماثل.
و (CH3CO)2أو أنه متماثل ، منذ R1= ص2 = CH3. مشتق من حمض الخليك أو الإيثانويك ، لذلك اسمه ، يتبع التفسير السابق: أنهيدريد الخل أو الإيثانويك. الشيء نفسه ينطبق على أنهيدريد الفثاليك المذكورة للتو.
افترض أن لديك الانهيدريد التالي:
CH3CO (O) COCH2CH2CH2CH2CH2CH3
تأتي مجموعة الأسيتيل الموجودة على اليسار من حمض الأسيتيك ، بينما تأتي المجموعة الموجودة على اليمين من حامض الهيبتانويك. لتسمية هذا الأنهيدريد ، يجب عليك تسمية مجموعات البحث بالترتيب الأبجدي. لذلك ، اسمها: أنهيدريد الخل الخلوي.
تطبيقات
تحتوي الأنهيدريدات غير العضوية على عدد لا نهائي من التطبيقات ، بدءًا من تخليق وصياغة المواد ، والسيراميك ، والعوامل الحفازة ، والإسمنت ، والأقطاب الكهربائية ، والأسمدة ، وما إلى ذلك ، إلى طلاء قشرة الأرض بآلافها من معادن الحديد والألومنيوم وثاني أكسيدها. من الزفير من الكائنات الحية.
إنها تمثل مصدر الانطلاق ، وهي النقطة التي تستمد منها العديد من المركبات المستخدمة في التخليق غير العضوي. واحدة من أهم أنهيدريد هو ثاني أكسيد الكربون ، أول أكسيد الكربون2. إنه ، مع الماء ، ضروري لعملية التمثيل الضوئي. وعلى المستوى الصناعي ، SO3 إنه أمر بالغ الأهمية لأن المدعى عليه يحصل على حامض الكبريتيك منه.
ربما يكون الأنهيدريد الذي يحتوي على مزيد من التطبيقات وله (ما دامت الحياة) واحدًا من حمض الفوسفوريك: أدينوسين ثلاثي الفوسفات ، المعروف باسم ATP ، الموجود في الحمض النووي و "العملة النشطة" لعملية التمثيل الغذائي.
أنهيدريد عضوي
يتفاعل أنهيدريد الحمض بواسطة أسيل ، إما إلى كحول ، أو تشكيل إستر ، إلى أمين ، مما يؤدي إلى أميد ، أو حلقة عطرية.
هناك الملايين من كل من هذه المركبات ، ومئات الآلاف من خيارات حمض الكربوكسيل لتحضير أنهيدريد ؛ لذلك ، فإن الاحتمالات الاصطناعية تنمو بشكل كبير.
وبالتالي ، فإن أحد التطبيقات الرئيسية هو دمج مجموعة الأسيل في مركب ، والاستعاضة عن إحدى الذرات أو مجموعات بنيتها.
لكل أنهيدريد على حدة تطبيقاته الخاصة ، ولكن بشكل عام ، كلها تتفاعل بطريقة مماثلة. لهذا السبب ، يتم استخدام هذه الأنواع من المركبات لتعديل هياكل البوليمر ، وإنشاء بوليمرات جديدة ؛ وهذا هو ، البوليمرات المشتركة ، والراتنجات ، والطلاء ، الخ.
على سبيل المثال ، يستخدم أنهيدريد الخل في أسيتيل جميع مجموعات OH من السليلوز (الصورة السفلية). مع هذا ، يتم استبدال كل H من OH بمجموعة الأسيتيل ، COCH3.
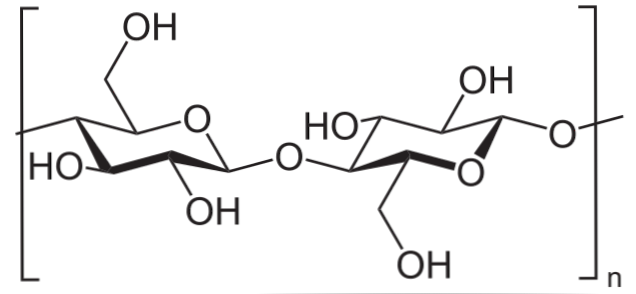
بهذه الطريقة يتم الحصول على بوليمر خلات السليلوز. يمكن رسم نفس التفاعل مع هياكل بوليمر أخرى مع مجموعات NH2, عرضة أيضا للاسيل.
تفاعلات الألكيل مفيدة أيضًا لتخليق العقاقير ، مثل الأسبرين (الحمض) الاسيتيلالصفصاف).
أمثلة
وتظهر بعض الأمثلة الأخرى من أنهيدريد العضوية في النهاية. على الرغم من عدم ذكر أي ذكر لها ، يمكن استبدال ذرات الأكسجين بالكبريت ، أو إعطاء الكبريت ، أو حتى أنهيدريد الفسفور.
-C6H5CO (O) COC6H5: أنهيدريد البنزويك. المجموعة ج6H5 يمثل حلقة البنزين. تنتج عملية التحلل المائي اثنين من الأحماض البنزويك.
-HCO (O) COH: أنهيدريد الفورميك. تنتج عملية التحلل المائي اثنين من الأحماض الفورمية.
- C6H5CO (O) COCH2CH3: البنزويك أنهيدريد البروبانويك. تنتج عملية التحلل المائي أحماض البنزويك والبروبانويك.
-C6H11CO (O) COC6H11: أنهيدريد سيكلوهكساني كربوكسيل على عكس الحلقات العطرية ، هذه مشبعة ، دون روابط مزدوجة.
-CH3CH2CH2CO (O) COCH2CH3: أنهيدريد البروتانويك.
أنهيدريد السكسينيك

هنا لدينا دوري آخر ، مشتق من حمض السكسينيك ، وحامض الكربوكسيل. لاحظ كيف تخون ذرات الأكسجين الثلاثة الطبيعة الكيميائية لهذا النوع من المركبات.
يشبه أنهيدريد المالئيك أنهيدريد السكسينيك ، مع وجود فرق مزدوج بين الكربونات التي تشكل أساس البنتاغون..
أنهيدريد الجلوتاري
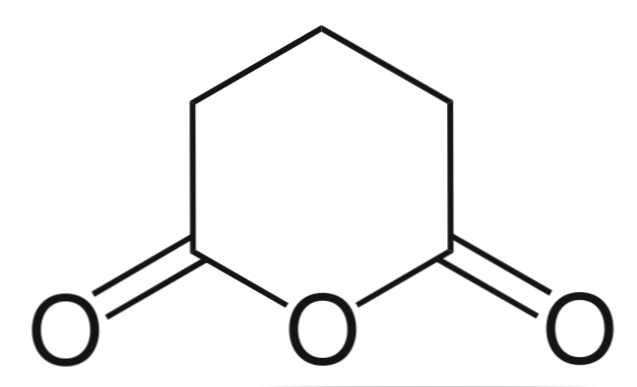
وأخيرًا يظهر أنهيدريد حمض الجلوتاريك. يتميز هذا هيكليا عن جميع الآخرين من خلال تتكون من حلقة سداسية. مرة أخرى ، تبرز ذرات الأكسجين الثلاثة في الهيكل.
يمكن دائمًا إثبات أنهيدريدات أخرى ، أكثر تعقيدًا ، بواسطة ذرات الأكسجين الثلاثة القريبة جدًا من بعضها البعض.
مراجع
- محرري الموسوعة البريطانية. (2019). أنهيدريد. Encryclopaedia Britannica. تم الاسترجاع من: britannica.com
- Helmenstine ، آن ماري ، دكتوراه (8 يناير 2019). تعريف أنهيدريد الحمض في الكيمياء. تم الاسترجاع من: thinkco.com
- كيمياء LibreTexts. (بدون تاريخ). المركبات الحمضية اثنين. تم الاسترجاع من: chem.libretexts.org
- غراهام سولومونز تي. دبليو ، كريج بي فرايل. (2011). الكيمياء العضوية. الأمينات. (10عشر طبعة). وايلي بلس.
- كاري ف. (2008). الكيمياء العضوية (الطبعة السادسة). مولودية جراو هيل.
- بياض ، ديفيس ، بيك وستانلي. (2008). الكيمياء. (الطبعة الثامنة). CENGAGE التعلم.
- موريسون و بويد. (1987). الكيمياء العضوية (الطبعة الخامسة). أديسون ويسلي Iberoamericana.
- ويكيبيديا. (2019). أنهيدريد حمض عضوي. تم الاسترجاع من: en.wikipedia.org


